微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (12分)硅孔雀石是一种含铜矿石,含铜形态为CuCO3、Cu(OH)2和CuSiO3?2H2 O,同时含有SiO2、FeCO3、Fe2O3、A12O3等杂质。以其为原料制取硫酸铜的工艺流程如下图所示:

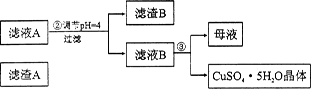
(1)步骤1中先加入足量稀硫酸,再加人双氧水。则双氧水参与该反应的离子方程式是_________________。
(2)步骤②调节溶液pH,可以选用的试剂是________。(填字母编号)
A.A12O3 B.CuO C.CuCO3・Cu(OH)2
(3)有关氢氧化物开始沉淀和完全沉淀的pH如下表:
氢氧化物
| Al(OH)3
| Fe(OH)3
| Fe(OH)2
| Cu(OH)2
|
开始沉淀的pH
| 3.3
| 1.5
| 6.5
| 4.2
|
沉淀完全的pH
| 5.2
| 3.7
| 9.7
| 6.7
|
则滤液B中含有的阳离子是__________________________。
(4)将滤液B通过_______、________、过滤等操作可得到硫酸铜晶体。
(5)硫酸铜也可用硫化铜和氧气在高温、催化剂条件下化合制得,该反应的化学方程式是______________。取384g CuS在一定条件下和氧气完全反应,若发生2CuS+3O2=2CuO+2SO2和4CuS+5O2=2Cu2O+4SO2两个反应,在所得固体中Cu和O的物质的量之比n(Cu):n(O)=4:a,此时消耗空气的物质的量为bmol。则a=__________。(氧气占空气体积的五分之一)
填空题 (12分)硅孔雀石是一种含铜矿石,含铜形态为CuCO3、Cu(OH)2和CuSiO3?2H2O,同时含有SiO2、FeCO3、Fe2O3、A12O3等杂质。以其为原料制取硫酸铜的工艺流程如下图所示:

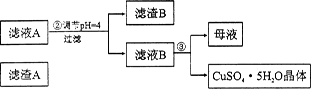
(1)步骤1中先加入足量稀硫酸,再加人双氧水。则双氧水参与该反应的离子方程式是_________________。
(2)步骤②调节溶液pH,可以选用的试剂是________。(填字母编号)
A.A12O3 B.CuO C.CuCO3・Cu(OH)2
(3)有关氢氧化物开始沉淀和完全沉淀的pH如下表:
氢氧化物
| Al(OH)3
| Fe(OH)3
| Fe(OH)2
| Cu(OH)2
|
开始沉淀的pH
| 3.3
| 1.5
| 6.5
| 4.2
|
沉淀完全的pH
| 5.2
| 3.7
| 9.7
| 6.7
|
则滤液B中含有的阳离子是__________________________。
(4)将滤液B通过_______、________、过滤等操作可得到硫酸铜晶体。
(5) 硫酸铜也可用硫化铜和氧气在高温、催化剂条件下化合制得,该反应的化学方程式是______________。取384g CuS在一定条件下和氧气完全反应,若发生2CuS+3O2=2CuO+2SO2和4CuS+5O2=2Cu2O+4SO2两个反应,在所得固体中Cu和O的物质的量之比n(Cu):n(O)=4:a,此时消耗空气的物质的量为bmol。则a=__________。(氧气占空气体积的五分之一)
本题答案:(1)2Fe2++H2O2+2H+=2Fe3++2H2O;(
本题解析:
试题分析:(1)步骤1中先加入足量稀硫酸,可以使盐溶解,再加入双氧水,可以把溶液中Fe2+氧化为Fe3+。根据电子转移数目相等可知:双氧水参与该反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O;(2)步骤②调节溶液pH,应该既可以消耗溶液中H+,同时也不引入杂质离子,因此加入的物质应该是含有Cu元素的化合物,因此是CuO、CuCO3・Cu(OH)2,选项是B、C;(3)由于Al(OH)3沉淀完全的pH是5.2;Fe(OH)3沉淀完全的pH是3.7;Cu(OH)2沉淀完全的pH是6.7,而控制的溶液pH=4,所以滤液B中含有的阳离子是Al3+、H+、Cu2+;(4)将滤液B通过蒸发浓缩、冷却结晶、过滤等操作可得到硫酸铜晶体。(5)用硫化铜和氧气在高温、催化剂条件下化合制得硫酸铜,根据元素原子守恒和电子守恒,可得该反应的化学方程式是CuS+2O2 CuSO4;n(O2)=
CuSO4;n(O2)= ;n(CuS)= 384g÷96g/mol=4mol。假设发生反应产生n(CuO)=xmol;n(Cu2O)=ymol,则根据元素守恒可得:x+2y=4mol;3x/2+5y/2=
;n(CuS)= 384g÷96g/mol=4mol。假设发生反应产生n(CuO)=xmol;n(Cu2O)=ymol,则根据元素守恒可得:x+2y=4mol;3x/2+5y/2= 。(x+2y):(x+y)= 4:a。整理可得x=4b/5-20;y=12-2b/5;a=
。(x+2y):(x+y)= 4:a。整理可得x=4b/5-20;y=12-2b/5;a=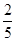 b-8。
b-8。
考点:考查离子方程式的书写、调整溶液pH的试剂的选用、溶液成分和混合物的成分的确定的知识。
本题所属考点:【有关氧化还原反应的计算】
本题难易程度:【困难】
Hope is bad for the happy man,and good for the unhappy. 希望对幸福的人是不好的事,对不幸福的人是好事.