微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 金属钛(Ti)性能优越,被称为继铁、铝后的“第三金属”。工业上以金红石为原料制取Ti的反应为aTiO2+bCl2+cC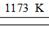 aTiCl4+cCO反应(1) TiCl4+2Mg
aTiCl4+cCO反应(1) TiCl4+2Mg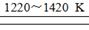 Ti+2MgCl2反应(2)
Ti+2MgCl2反应(2)
关于反应(1)、(2)的分析不正确的是
①TiCl4在反应(1)中是还原产物,在反应(2)中是氧化剂;
②C、Mg在反应中均为还原剂,被还原;
③在反应(1)、(2)中的还原性C>TiCl4,Mg> Ti;
④a=1,b=c=2;
⑤每生成19.2 g Ti(Mr=48),反应(1)、(2)中共转移4.8 mol e-。
A. ①②④ B. ②③④ C. ③④ D. ②⑤
选择题 金属钛(Ti)性能优越,被称为继铁、铝后的“第三金属”。工业上以金红石为原料制取Ti的反应为aTiO2+bCl2+cC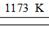 aTiCl4+cCO反应(1) TiCl4+2Mg
aTiCl4+cCO反应(1) TiCl4+2Mg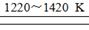 Ti+2MgCl2反应(2)
Ti+2MgCl2反应(2)
关于反应(1)、(2)的分析不正确的是
①TiCl4在反应(1)中是还原产物,在反应(2)中是氧化剂;
②C、Mg在反应中均为还原剂,被还原;
③在反应(1)、(2)中的还原性C>TiCl4,Mg>Ti;
④a=1,b=c=2;
⑤每生成19.2 g Ti(Mr=48),反应(1)、(2)中共转移4.8 mol e-。
A. ①②④ B. ②③④ C. ③④ D. ②⑤
本题答案:D
本题解析:
试题分析:①在反应(1)中氯元素的化合价降低,则TiCl4在反应(1)中是还原产物;在反应(2)中Ti的化合价从+4价降低到0价,是氧化剂,①正确;②C、Mg在反应中都失去电子,均为还原剂,被氧化,②错误;③在氧化还原反应中还原剂的还原性强于还原产物的还原性,则在反应(1)、(2)中的还原性C>TiCl4、Mg>Ti,③正确;④根据原子守恒和电子得失守恒可知在反应(1)中a=1,b=c=2,④正确;⑤19.2gTi的物质的量是19.2g÷48g/mol=0.4mol,根据反应式(2)可知转移电子的物质的量是0.4mol×4=1.6mol。生成0.4mol TiCl4相应消耗0.8mol氯气,则反应(1)中转移0.8mol×2=1.6mol电子,所以每生成19.2 g Ti(Mr=48),反应(1)、(2)中共转移3.2mol e-,⑤错误,答案选D。
考点:考查氧化还原反应的有关判断与计算
本题所属考点:【有关氧化还原反应的计算】
本题难易程度:【一般】
Every man has his faults. 人都有缺点.