| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
“神七”登天标志着我国的航天事业进入了新的篇章。(1)火?【未知】
该反应中被氧化的原子与被还原的原子的物质的量之比是 。这个反应应用于火箭推进器,除释放大量的热和快速产生大量气体外,还有一个很大的优点是 。 (3)如图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解液,燃料电池放电时的负极反应为: 。如果某段时间内氢氧储罐中共收集到33.6L气体(已折算成标况),则该段时间内水电解系统中转移电子的物质的量为 mol。 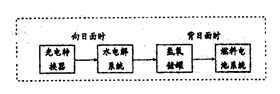 (4)在载人航天器的生态系统中,不仅要求分离去除CO2,还要求提供充足的O2。某种电化学装置可实现如下转化:2CO2=2CO+O2,CO可用作燃料。 已知该反应的阳极反应为:4OH―4e-=O2↑+2H2O 则阴极反应为: 。有人提出,可以设计反应2CO=2C+O2(△H>0、△S<0)来消除CO的污染。请你判断上述反应是否能发生? 理由 。 (5).北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。丙烷脱氢可得丙烯。 已知:①C3H8(g)  CH4(g)+HC≡CH(g)+H2(g); △H1="156.6" kJ・mol-1 CH4(g)+HC≡CH(g)+H2(g); △H1="156.6" kJ・mol-1②CH3CH=CH2(g)  CH4(g)+ HC≡CH (g);△H2="32.4" kJ・mol-1 CH4(g)+ HC≡CH (g);△H2="32.4" kJ・mol-1则相同条件下,反应C3H8(g)  CH3CH=CH2(g)+H2(g)的△H=_____kJ・mol-1 CH3CH=CH2(g)+H2(g)的△H=_____kJ・mol-1 填空题 “神七”登天标志着我国的航天事业进入了新的篇章。 | A.在高温下不融化 | B.在高温下可分解气化 | |||||
| C.在常温下就分解气化 | D.该涂料不可能发生分解 |

 CH4(g)+HC≡CH(g)+H2(g); △H1="156.6" kJ・mol-1
CH4(g)+HC≡CH(g)+H2(g); △H1="156.6" kJ・mol-1 CH4(g)+ HC≡CH (g);△H2="32.4" kJ・mol-1
CH4(g)+ HC≡CH (g);△H2="32.4" kJ・mol-1 CH3CH=CH2(g)+H2(g)的△H=_____kJ・mol-1
CH3CH=CH2(g)+H2(g)的△H=_____kJ・mol-1 CH3CH=CH2(g)+H2(g)的△H=124.2KJ/mol.
CH3CH=CH2(g)+H2(g)的△H=124.2KJ/mol.本题所属考点:【未知】
本题难易程度:【困难】
|
||
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | ||
| 下一篇:请将5种物质:N2O、FeCl2、Fe (NO.. | ||