|
|
|
(18分)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型【未知】
2016-12-27 14:21:28
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (18分)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能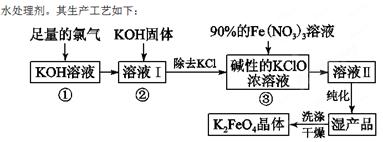
(1)反应①应在温度较低的情况下进行。因在温度较高时KOH与Cl2反应生成的是KClO3。写出在温度较高时KOH与Cl2反应的化学方程式 ,该反应的氧化产物是 。
(2)在溶液Ⅰ中加入KOH固体的目的是 (填编号)。
A.与溶液Ⅰ中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供碱性的环境
D.使KClO3转化为KClO
| (3)从溶液Ⅱ中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为 。
(4)如何判断K2FeO4晶体已经洗涤干净 。
(5)高铁酸钾(K2FeO4)作为水处理来源:91考试网 91Exam.org剂的一个优点是能与水反应生成胶体吸附杂质,配平该反应的离子方程式:
___FeO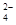 +____H2O ― ____Fe(OH)3(胶体)+____O2↑+____OH-。 +____H2O ― ____Fe(OH)3(胶体)+____O2↑+____OH-。
填空题 (18分)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能
(1)反应①应在温度较低的情况下进行。因在温度较高时KOH与Cl2反应生成的是KClO3。写出在温度较高时KOH与Cl2反应的化学方程式 ,该反应的氧化产物是 。
(2)在溶液Ⅰ中加入KOH固体的目的是 (填编号)。
A.与溶液Ⅰ中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一 91ExAM.org步反应提供碱性的环境
D.使KClO3转化为KClO
|
(3)从溶液Ⅱ中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为
。
(4)如何判断K2FeO4晶体已经洗涤干净
。
(5)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,配平该反应的离子方程式:
___FeO
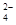
+
____H2O ―
____Fe(OH)3(胶体)+
____O2↑+
____OH-。
本题答案:(1)6KOH+3Cl2
据题目信息、氧化还原反应中化合价发生变化确定产物有:KClO3、KCl、H2O,根据电子得失守恒和质量守恒来配平,可得6KOH+3Cl2<img onload='if(this.width>600)makesmallpic(this,600,1800);' src=)
KClO3+5KCl+3H2O;Cl2既是氧化剂又是还原剂,氯化合价升高,得到 KClO3,KClO3是还原产物。
(2)A、根据生产工艺流程图,第①步氯气过量,加入KOH固体后会继续反应生成KClO,正确;B、因温度较高时KOH 与Cl2 反应生成的是KClO3,而不是KClO,错误; C、第③步需要碱性条件,所以碱要过量,正确;D、KClO3转化为 KClO,化合价只降不升,错误。
(3)据题目信息和氧化还原反应中化合价发生变化确定找出反应物:Fe3+、ClO-,生成物:FeO42-、Cl-,根据电子得失守恒和质量守恒来配平,可得2Fe3++3ClO-+10OH-=2FeO42-+
3Cl-+5H2O
(4)因只要检验最后一次的洗涤中无Cl-,即可证明K2FeO4晶体已经洗涤干净,所以检验方法为:用试管取少量最后一次的洗涤液,加入硝酸银溶液,无白色沉淀则已被洗净。
(5)根据电子得失守恒和质量守恒来配平,可得4FeO42-+10H2O
本题所属考点:【未知】
本题难易程度:【困难】
No man is a hero to his valet. 在最贴身的人眼中,谁也充不了伟人。
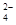 +____H2O ― ____Fe(OH)3(胶体)+____O2↑+____OH-。
+____H2O ― ____Fe(OH)3(胶体)+____O2↑+____OH-。 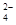 +____H2O ― ____Fe(OH)3(胶体)+____O2↑+____OH-。
+____H2O ― ____Fe(OH)3(胶体)+____O2↑+____OH-。