|
|
|
铬铁矿的主要成分的化学式为FeO・Cr2O3,还含有SiO2、Al2O3等杂?【未知】
2016-12-27 14:25:06
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 铬铁矿的主要成分的化学式为FeO・Cr2O3,还含有SiO2、Al2O3等杂质。工业上常采用固体碱熔氧化法用铬铁矿粉制备重铬酸钾,流程为:
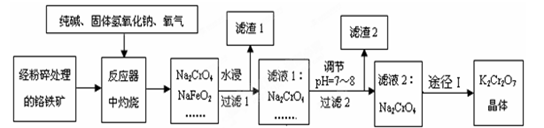
已知:①NaFeO2遇水强烈水解;
②重铬酸钾为橙红色针状晶体,溶于水,不溶于乙醇,有强氧化性;
③2CrO42- + 2H+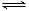 Cr2O72-+ H2O Cr2O72-+ H2O
(1)灼烧操作一般在坩埚中进行,下列物质适合用来制作此实验坩埚材料的是
A.铁
B.氧化铝
C.石英
D.陶瓷
| (2)①铬铁矿经粉碎处理的目的是 ; 。
②写出Cr2O3和纯碱、氧气反应生成Na2CrO4的化学方程式为 ;
③NaFeO2水浸时强烈水解生成氢氧化铁沉淀,离子方程式为___ ___。
(3)滤液1的成分除Na2CrO4、NaOH外,还含有(填化学式) ,
(4)通过途径Ⅰ从Na2CrO4溶液获得K2Cr2O7晶体,操作步骤有:“酸化”→加KCl固体→蒸发浓缩→操作a→过滤→洗涤→干燥。
① “酸化”步骤用醋酸调节溶液pH<5,其目的是 ;
②操作a的名称 。
填空题 铬铁矿的主要成分的化学式为FeO・Cr2O3,还含有SiO2、Al2O3等杂质。工业上常采用固体碱熔氧化法用铬铁矿粉制备重铬酸钾,流程为:

已知:①NaFeO2遇水强烈水解;
②重铬酸钾为橙红色针状晶体,溶于水,不溶于乙醇,有强氧化性;
③2CrO42- + 2H+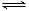 Cr2O72-+ H2O Cr2O72-+ H2O
(1)灼烧操作一般在坩埚中进行,下列物质适合用来制作此实验坩埚材料的是
A.铁
B.氧化 铝
C.石英
D.陶瓷
|
(2)①铬铁矿经粉碎处理的目的是
。
②写出Cr2O3和纯碱、氧气反应生成Na2CrO4的化学方程式为
;
③NaFeO2水浸时强烈水解生成氢氧化铁沉淀,离子方程式为___
___。
(3)滤液1的成分除Na2CrO4、NaOH外,还含有(填化学式)
,
(4)通过途径Ⅰ从Na2CrO4溶液获得K2Cr2O7晶体,操作步骤有:“酸化”→加KCl固体→蒸发浓缩→操作a→过滤→洗涤→干燥。
① “酸化”步骤用醋酸调节溶液pH<5,其目的是
;
②操作a的名称
。
本题答案:(1)A ( 3分)
(2)① 增大反应物的表面积,加
本题解析:
试题分析:(1)陶瓷中含二氧化硅,石英的作用成分是二氧化硅,氢氧化钠与氧化铝、二氧化硅反应,所以适合用来制作此实验坩埚材料的是铁,答案选A;
(2)①粉碎固体使其与反应物的接触面积增大,加快反应速率;
② 根据元素守恒判断Cr2O3和纯碱、氧气反应生成Na2CrO4和二氧化碳,化学方程式为
2Cr2O3 + 3O2+4Na2CO3

4Na2CrO4+4CO2↑;
③ NaFeO2水浸时强烈水解生成氢氧化铁沉淀,书写离子方程式时可逆符号变为“=”,离子方程式为
FeO2-+2H2O=Fe(OH)3↓+OH-
(3)SiO2、Al2O3等杂质与氢氧化钠反应生成硅酸钠、偏铝酸钠,所以滤液1的成分除Na2CrO4、NaOH外,还含有NaAlO2 、Na2SiO3
(4)①根据已知③Na2CrO4溶液中存在2CrO42- + 2H+
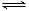
Cr2O72-+ H2O平衡,加入醋酸调节pH<5,使平衡正向移动,尽量将CrO42-转化为Cr2O72-
②由溶液得到晶体的一般步骤是加热浓缩、冷却结晶、过滤、洗涤、干燥,所以本实验中加热浓缩后应冷却结晶。
考点:考查仪器的选择、实验步骤的判断,根据题目信息书写化学方程式、离子方程式、物质成分的判断
本题所属考点:【未知】
本题难易程度:【一般】
It is as well to know which way the wind blows. 最好知道风吹往哪个方向。识时务者为俊杰。
 4Na2CrO4+4CO2↑;
4Na2CrO4+4CO2↑;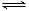 Cr2O72-+ H2O平衡,加入醋酸调节pH<5,使平衡正向移动,尽量将CrO42-转化为Cr2O72-
Cr2O72-+ H2O平衡,加入醋酸调节pH<5,使平衡正向移动,尽量将CrO42-转化为Cr2O72-