微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的
关系如图 所示。
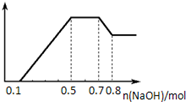
则下列说法正确的是
A.溶液中一定不含CO32-,可能含有SO42-和NO3-
B.溶液中的阳离子只有H+、Mg2+、Al3+
C.溶液中n(NH4+)="0.2mol"
D.n(H+)∶n(Al3+)∶n(Mg2+) = 1∶1∶1
选择题 某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶 液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的
关系如图所示。

则下列说法正确的是
A.溶液中一定不含CO32-,可能含有SO42-和NO3-
B.溶液中的阳离子只有H+、Mg2+、Al3+
C.溶液中n(NH4+)="0.2mol"
D.n(H+)∶n(Al3+)∶n(Mg2+) = 1∶1∶1
本题答案:C
本题解析:
试题分析:加入锌粒,产生无色无味的气体,则该溶液含有H+,不含CO32?;根据图像白色沉淀的量先增加,然后不变,然后溶解一部分,说明该溶液含Al3+、Mg2+、NH4+,不含Fe3+,SO42?与NO3?至少含有一种,故A、B错误;加入NaOH0.5mol至0.7mol时与NH4+反应,NH4++OH?=NH3?H2O,则NH4+物质的量为0.2mol,故C正确;D、加入NaOH0~0.1mol,与H+反应,则H+为0.1mol,加入NaOH0.7mol~0.8mol,与Al(OH)3反应,Al(OH)3+OH?=[Al(OH)4]?,则Al(OH)3、Al3+物质的量为0.1mol,根据Al3++3OH?=Al(OH)3↓,生成Al(OH)3需要NaOH0.3mol,加入NaOH0.1至0.5mol,生成Al(OH)3、Mg(OH)2,则生成Mg(OH)2需要NaOH物质的量为:0.4mol-0.3mol=0.1mol,根据Mg2++2OH?=Mg(OH)2↓,可得Mg2+物质的量为0.05mol,所以n(H+)∶n(Al3+)∶n(Mg2+) = 2∶2∶1,故D项错误。
考点:本题考查离子反应、图像的分析、化学计算。
本题所属考点:【离子共存】
本题难易程度:【困难】
Man aspires after happiness and trees wait for the advent of spring. 人望幸福树望春.