微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (10分)某强酸性溶液X含有Ba2+、Al3+、NH 、Fe2+、Fe3+、CO
、Fe2+、Fe3+、CO 、SO
、SO 、SO
、SO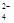 、Cl-、NO
、Cl-、NO 中的一种或几种,取该溶液进行实验,实验内容如下:
中的一种或几种,取该溶液进行实验,实验内容如下:

根据以上信息,回答下列问题:
(1)溶液X中除H+外还肯定含有的离子是____________________________ _________;
(2)写出有关离子方程式:
步骤①中生成A__________________;步骤②生成沉淀I__________________。
(3)假设测定A、F、I均为0.01 mol,10 mL X溶液中n(H+)=0.04 mol,而沉淀C物质的量0.07 mol,能说明该溶液不能确定的阴离子存在的理由是___________________。
填空题 (10分)某强酸性溶液X含有Ba2+、Al3+、NH 、Fe2+、Fe3+、CO
、Fe2+、Fe3+、CO 、SO
、SO 、SO
、SO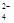 、Cl-、NO
、Cl-、NO 中的一种或几种,取该溶液进行实验,实验内容如下:
中的一种或几种,取该溶液进行实验,实验内容如下:

根据以上信息,回答下列问题:
(1)溶液X中除H+外还肯定含有的离子是_____________________________________;
(2)写出有关离子方程式:
步骤①中生成A__________________;步骤②生成沉淀I__________________。
(3)假设测定A、F、I均为0.01 mol,10 mL X溶液中n(H+)=0.04 mol,而沉淀C物质的量0.07 mol,能说明该溶液不能确定的阴离子存在的理由是___________________。
本题答案:(1)Fe2+、SO42-、NH4+、Al3+;
(2
本题解析:
试题分析:由题干知该溶液为强酸性溶液所以CO32-、SO32-一定不存在;由流程图中信息可知:加过量Ba(NO3)2生成气体A为NO,气体D为NO2,溶液E为HNO3溶液,可判定原溶液一定有Fe2+,一定无NO3-;由此可推断沉淀G为Fe(OH)3;加过量Ba(NO3)2生成沉淀C为BaSO4,则原溶液中一定有SO42-无Ba2+;
加过量NaOH溶液生成气体F为NH3,则溶液中一定有NH4+;通入过量CO2时生成沉淀I为Al(OH)3,则原溶液中一定有Al3+,若NO、NH3、Al(OH)3均为0.01 mol、BaSO4为0.07 mol,综合上述分析可知10 mL X溶液中Fe2+、NH4+、Al3+、SO42-的物质的量各为0.03mol、0.01mol、0.01mol、0.07 mol;又知10 mL X溶液中n(H+)=0.04 mol,恰好符合电荷守恒因此如果可以测定原溶液中还有Fe3+则有Cl-,否则没有Cl-.
考点:了解离子反应的概念、离子反应发生的条件。了解常见离子的检验方法。
点评:熟练掌握离子的性质进行离子检验,同时也要注意离子间的量的关系如第(3)题中应用电解质溶液中的电荷守恒关系。
本题所属考点:【离子共存】
本题难易程度:【困难】
Love is all very well in its way, but friendship is much higher. 爱情自有其美好处,可是友谊更可贵.