微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (12分).铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等。回答下列问题:
(1)铅是碳的同族元素,比碳多4个电子层,铅在元素周期表的位置为 ; ,
PbO2的酸性比CO2的酸性 (填“强”或“弱”)。
(2)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为 。
(3)PbO2可由PbO与次氯酸钠溶液反应制得反应的离子方程式为 ;
PbO2也可以通过石墨为电极Pb(NO3)2和Cu(NO3)2的混合溶液为电解液电解制取。阳极发生的电极反应式为_ _。若电解液中不加入Cu(NO3)2,主要缺点是 。
(4)PbO2在加热过程发生分解的失重曲线如下图所示,已知失重曲线上的a点为样品失重4.0%(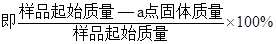 )的残留固体,若a点固体组成表示为PbOX或mPbO2・nPbO,列式计算x值和m:n值_ 。
)的残留固体,若a点固体组成表示为PbOX或mPbO2・nPbO,列式计算x值和m:n值_ 。
填空题 (12分).铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等。回答下列问题:
(1)铅是碳的同族元素,比碳多4个电子层,铅在元素周期表的位置为 ,
PbO2的酸性比CO2的酸性 (填“强”或“弱”)。
(2)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为 。
(3)PbO2可由PbO与次氯酸钠溶液反应制得反应的离子方程式为 & #160; ;
PbO2也可以通过石墨为电极Pb(NO3)2和Cu(NO3)2的混合溶液为电解液电解制取。阳极发生的电极反应式为_ _。若电解液中不加入Cu(NO3)2,主要缺点是 。
(4)PbO2在加热过程发生分解的失重曲线如下图所示,已知失重曲线上的a点为样品失重4.0%(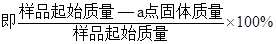 )的残留固体,若a点固体组成表示为PbOX或mPbO2・nPbO,列式计算x值和m:n值_ 。
)的残留固体,若a点固体组成表示为PbOX或mPbO2・nPbO,列式计算x值和m:n值_ 。
本题答案:(12分)(第1小题每空1分,其余每空2分)
(1)
本题解析:
试题分析:(1)Pb在元素周期表中位于第六周期第ⅣA族,根据元素周期律可知,同主族元素从上到下,元素的非金属性逐渐减弱,所以PbO2的酸性比CO2的酸性弱;
(2)PbO2与浓盐酸共热生成黄绿色气体,该黄绿色气体是氯气,说明Cl元素被氧化,则Pb元素被还原为Pb2+,反应的化学方程式为PbO2+4HCl(浓)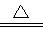 PbCl2+Cl2↑+2H2O;
PbCl2+Cl2↑+2H2O;
(3)PbO与次氯酸钠溶液反应制得PbO2,Pb元素被氧化,则Cl元素被还原为氯离子,离子方程式为PbO+ClO―= PbO2+Cl-;石墨为电极Pb(NO3)2和Cu(NO3)2的混合溶液为电解液电解制取PbO2,阳极发生氧化反应,则Pb2+失去2个电子生成+4价的PbO2,根据元素守恒,发生反应的离子方程式为:Pb2++2H2O - 2e-= PbO2↓+ 4H+,若电解液中不加入Cu(NO3)2,阴极上Pb2+获得电子生成Pb,阴极电极反应式为:Pb2++2e-=Pb↓,Pb2+的利用率降低;
(4)若a点固体组成表示为PbOx,根据PbO2 PbO
PbO +
+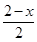 O2↑,设开始有1mol PbO2固体,质量是239g,则a点有
O2↑,设开始有1mol PbO2固体,质量是239g,则a点有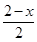 ×32=
×32=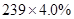 ,解得x=1.4,则mPbO2・nPbO中O原子的个数平均是1.4,所以(2m+n)/(m+n)=1.4,m:n=2:3.
,解得x=1.4,则mPbO2・nPbO中O原子的个数平均是1.4,所以(2m+n)/(m+n)=1.4,m:n=2:3.
考点:考查元素周期表与元素周期律、常用化学用语、电解原理、方程式的计算
本题所属考点:【离子方程式的书写及正误判断】
本题难易程度:【困难】
All is not gain that is got into the purse. 装进钱包里的不一定都是收益.