微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (16分)某工厂的废金属屑中主要成分为Cu、Fe和Al,此外还含有少量Al2O3和Fe2O3,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体(FeSO4・7H2O)和胆矾晶体。
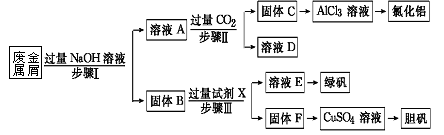
请回答:
(1)写出步骤Ⅰ反应的离子方程式: ; 。
(2)试剂X是 。由溶液D是 。
(3)在步骤Ⅱ时,用如图装置制取CO2并通入溶液A中。
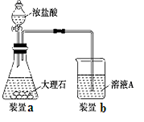
一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为了避免固体C减少,可采取的改进措施是 。
(4)溶液E中加入KSCN溶液无明显现象,表明滤液中不存在Fe3+,用离子方程式解释其可能的原因 。
(5)用固体F继续加入热的稀H2SO4,同时不断鼓入空气,固体溶解得CuSO4溶液;写出反应的化学方程式 ,
(6)工业上常用溶液E经进一步处理可制得净水剂Na2FeO4,流程如下:
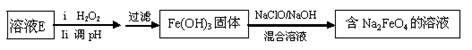
①测得溶液E中c(Fe2+) 为0.2 mol・L-1,若要处理1 m3溶液E,理论上需要消耗25 % 的H2O2溶液___kg。
②写出由Fe(OH)3制取Na2FeO4的离子方程式___________。
填空题 (16分)某工厂的废金属屑中主要成分为Cu、Fe和Al,此外还含有少量Al2O3和Fe2O3,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体(FeSO4・7H2O)和胆矾晶体。

请回答:
(1)写出步骤Ⅰ反应的离子方程式: ; 。
(2)试剂X是 。由溶液D是 。
(3)在步骤Ⅱ时,用如图装置制取CO2并通入溶液A中。

一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为了避免固体C减少,可采取的改进措施是 。
(4)溶液E中加入KSCN溶液无明显现象,表明滤液中不存在Fe3+,用离子方程式解释其可能的原因 。
(5)用固体F继续加入热的稀H2SO4,同时不断鼓入空气,固体溶解得CuSO4溶液;写出反应的化学方程式 ,
(6)工业上常用溶液E经进一步处理可制得净水剂Na2FeO4,流程如下来源:91exam .org:

①测得溶液E中c(Fe2+) 为0.2 mol・L-1,若要处理1 m3溶液E,理论上需要消耗25 % 的H2O2溶液___kg。
②写出由Fe(OH)3制取Na2FeO4的离子方程式___________。
本题答案:(1)2Al+2H2O+2OH-=2AlO2-+3H2↑&#
本题解析:
试题分析:(1)在废金属屑中含有Cu、Fe、Al、Al2O3、Fe2O3,当加入过量NaOH溶液时,只有Al、Al2O3可以发生反应,所以步骤Ⅰ反应的离子方程式是2Al+2H2O+2OH-=2AlO2-+3H2↑ ; Al2O3+ 2OH-= 2AlO2-+H2O;(2)把混合物过滤,得到的固体B中含有Cu、Fe、Fe2O3,向其中加入过量的稀硫酸,发生反应:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;Fe2(SO4)3+Fe= 3FeSO4;Fe2(SO4)3+Cu= 2FeSO4+ CuSO4 ; Fe+ H2SO4=FeSO4+H2↑;试剂X是H2SO4;过滤得到滤液E含有FeSO4、CuSO4;固体F中含有Cu,用热的浓硫酸溶解得到CuSO4溶液,也可以用固体F继续加入热的稀H2SO4,同时不断鼓入空气,固体溶解得CuSO4溶液;(3)溶液A中含有NaOH、NaAlO2;向其中通入过量的CO2,发生反应产生Al(OH)3沉淀和可溶性物质NaHCO3,溶液D是NaHCO3,固体C是Al(OH)3沉淀,用盐酸溶解得到AlCl3;然后在HCl的气氛中加热蒸发得到无水AlCl3;(3)在步骤Ⅱ时,用如图装置制取CO2并通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少,这是由于浓盐酸有挥发性,在制取的CO2气体中含有杂质HCl。为了避免固体C减少,可采取的改进措施是a,b间加一个盛有饱和NaHCO3的洗气瓶,除去HCl;(4)溶液E中加入KSCN溶液无明显现象,表明滤液中不存在Fe3+,是因为Fe3+有氧化性,发生了反应2Fe3++Fe=3Fe2+,变为Fe2+,(5)用固体F继续加入热的稀H2SO4,同时不断鼓入空气,固体溶解得CuSO4溶液;反应的化学方程式是2Cu+O2+ 2H2SO4 2CuSO4+2H2O;(6)①Fe2+与H2O2反应的方程式是:2Fe2++H2O2+2H+= 2Fe3++2H2O,由于n(Fe2+)="0.2" mol/L×1×103 L=200mol,则根据方程式可知需要H2O2的物质的量是100mol,所以理论上需要消耗的H2O2溶液(100mol×34g/mol)÷25 %=13600g=13.6Kg;②根据图示可知由Fe(OH)3制取Na2FeO4的离子方程式是2Fe(OH)3+ 3NaClO+ 4NaOH=2Na2FeO4+3NaCl+5H2O。
2CuSO4+2H2O;(6)①Fe2+与H2O2反应的方程式是:2Fe2++H2O2+2H+= 2Fe3++2H2O,由于n(Fe2+)="0.2" mol/L×1×103 L=200mol,则根据方程式可知需要H2O2的物质的量是100mol,所以理论上需要消耗的H2O2溶液(100mol×34g/mol)÷25 %=13600g=13.6Kg;②根据图示可知由Fe(OH)3制取Na2FeO4的离子方程式是2Fe(OH)3+ 3NaClO+ 4NaOH=2Na2FeO4+3NaCl+5H2O。
考点:考查反应试剂的选择、物质成分的确定、实验操作方法、化学方程式和离子方程式的书写及有关化学方程式的计算的知识。
本题所属考点:【离子方程式的书写及正误判断】
本题难易程度:【困难】
Life is too short to waste. 生命短促,不容浪费.