微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 下列反应的方程式正确的是
A.H2S水溶液呈酸性:H2S= H++ HS-
B.醋酸钠溶液和硫酸氢钠混合:CH3COO-+H+=CH3COOH
C.向澄清石灰水中通入过量二氧化碳:Ca2++2OH-+CO2=CaCO3↓+H2O
D.碳酸钠溶液呈碱性:CO32-+2H2O=H2CO3+2OH-
选择题 下列反应的方程式正确的是
A.H2S水溶液呈酸性:H2S= H++HS-
B.醋酸钠溶液和硫酸氢钠混合:CH3COO-+H+=CH3COOH
C.向澄清石灰水中通入过量二氧化碳:Ca2++2OH-+CO2=CaCO3↓+H2O
D.碳酸钠溶液呈碱性:CO32-+2H2O=H2CO3+2OH-
本题答案:B
本题解析:
试题分析:A.H2S的二元弱酸,分步电离,在溶液中存在电离平衡,电离方程式是:H2S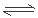 H++HS-错误;B.硫酸氢钠是强酸的酸式盐,在溶液中完全电离产生H+,醋酸钠溶液和硫酸氢钠混合:CH3COO-+H+=CH3COOH,正确;C.向澄清石灰水中通入过量二氧化碳,会产生碳酸氢钙,反应的两种方程式是:Ca2++OH-+CO2=Ca2++HCO3-,错误;D.碳酸钠溶液呈碱性,是由于CO32-在溶液中会发生水解反应存在水解平衡:CO32-+H2O
H++HS-错误;B.硫酸氢钠是强酸的酸式盐,在溶液中完全电离产生H+,醋酸钠溶液和硫酸氢钠混合:CH3COO-+H+=CH3COOH,正确;C.向澄清石灰水中通入过量二氧化碳,会产生碳酸氢钙,反应的两种方程式是:Ca2++OH-+CO2=Ca2++HCO3-,错误;D.碳酸钠溶液呈碱性,是由于CO32-在溶液中会发生水解反应存在水解平衡:CO32-+H2O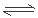 HCO3-+OH-,但是多元弱酸的酸根离子水解反应逐步进行,主要是第一步水解,错误。
HCO3-+OH-,但是多元弱酸的酸根离子水解反应逐步进行,主要是第一步水解,错误。
考点:考查反应的方程式正误判断的知识。
本题所属考点:【离子方程式的书写及正误判断】
本题难易程度:【困难】
Stuff today and starve tomorrow. 今日大鱼大肉,明日饥肠辘辘.