微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (1)3 mol KClO3完全分解,生成氧气的物质的量为 mol,其质量为 g。
(2) mol Zn和足量的HCl反应,生成氢气1.5 mol。
(3)与5.1 g某二元酸H2R完全反应,刚好消耗NaOH的质量为12 g,则H2R的摩尔质量为 。
填空题 (1)3 mol KClO3完全分解,生成氧气的物质的量为 mol,其质量为 g。
(2) mol Zn和足量的HCl反应,生成氢气1.5 mol。
(3)与5.1 g某二元酸H2R完全反应,刚好消耗NaOH的质量为12 g,则H2R的摩尔质量为 。
本题答案: (1)4.5 144 (2)1.5 (3)34 g・mol
本题解析:
试题分析:此3小题均为物质的量在化学方程式中的简单计算。将物质的量运用于方程式计算时,一定要明确物质的量与化学方程式的化学计量数间的关系,即化学计量数之比等于物质的量之比。
(1)反应式为2KClO3 2KCl+3O2↑,表示2 mol KClO3完全分解,生成3 mol氧气,若有3 mol KClO3完全分解,则生成4.5 mol氧气。此过程可列式如下:
2KCl+3O2↑,表示2 mol KClO3完全分解,生成3 mol氧气,若有3 mol KClO3完全分解,则生成4.5 mol氧气。此过程可列式如下:
2KClO3 2KCl+3O2↑
2KCl+3O2↑
2 mol & #160; 3 mol
3 mol n(O2)
n(O2)=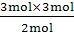 =4.5 mol,
=4.5 mol,
m(O2)=4.5 mol×32 g・mol-1="144" g。
(2)解题过程为
Zn+2HCl====ZnCl2+H2↑
1 mol 1 mol
n(Zn) 1.5 mol
n(Zn)=1.5 mol。
(3)本小题要求H2R的摩尔质量,需知道H2R的物质的量,而H2R的物质的量要根据与NaOH的反应来确定。解题过程为n(NaOH)=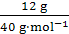 =0.3 mol。
=0.3 mol。
H2R + 2NaOH====Na2R+2H2O
1 mol 2 mol
n(H2R) 0.3 mol
n(H2R)=0.15 mol,
M(H2R)=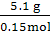 ="34" g・mol-1。
="34" g・mol-1。
考点:物质的量的计算、化学方程式计算。
本题所属考点:【物质的量】
本题难易程度:【一般】
You can't build a reputation on what you are going to do. 你不能靠你声称将要去做的事建立声誉.