|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 用锌片与稀硫酸反应,实验结果记录如表
次数
| 加入Zn质量/g
| 加入稀硫酸质量/g
| 生成ZnSO 4 质量/g
| 1
| 2
| 60
| 5
| 2
| 4
| 60
|
| 3
| 6
| 60
| 15
| 4
| 8
| 60
| 17
| 5
| 10
| 60
|
| 6
| 12
| 60
| 17
(1)第2、5两次产生ZnSO4 的质量依次是______________g.
(2)在图中画出ZnSO4 与Zn的质量函数关系的曲线.

(3)(10+m)g锌与60g稀硫酸充分反应后,剩余固体的质量为______________g.
(4)稀硫酸的溶质质量分数是______________.
填空题 用锌片与稀硫酸反应,实验结果记录如表
次数
| 加入Zn质量/g
| 加入稀硫酸质量/g
| 生成ZnSO 4 质量/g
| 1
| 2
| 60
| 5
| 2
| 4
| 60
|
| 3
| 6
| 60
| 15
| 4
| 8
| 60
| 17
| 5
| 10
| 60
|
| 6
| 12
| 60
| 17
(1)第2、5两次产生ZnSO4 的质量依次是______________g.
(2)在图中画出ZnSO4 与Zn的质量函数关系的曲线.

(3)(10+m)g锌与60g 稀硫酸充分反应后,剩余固体的质量为______________g.
(4)稀硫酸的溶质质量分数是______________.
本题答案:(1)10g、17g
(2)如图(若没有标
本题解析:
试题分析:根据表格中前4次的数据可以看出:硫酸的质量不变,Zn的质量增加,产生的ZnSO4 质量也逐渐增加,说明硫酸过量,原因第2次的质量是第一次的2倍,所以产生的ZnSO4质量也是第一次的2倍,质量是2×5g=10g;第四次产生ZnSO4质量是17g,第6次Zn质量增加,而产生的ZnSO4质量不变,说明硫酸反应完全,所以第5次加入Zn质量是10g时产生的ZnSO4质量也是17g;(2)65gZn完全反应会产生161g ZnSO4,则产生17g ZnSO4消耗的Zn的质量是:(17×65g)÷161=6.9g,则ZnSO4 与Zn的质量函数关系的曲线是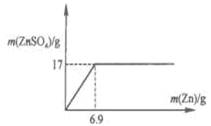 ; ;
(3)(10+m)g锌与60g稀硫酸充分反应后产生ZnSO4质量是17g,消耗Zn的质量是6.9gZn质量再增加,也不会发生反应,所以剩余固体的质量为(10+m)g-6.9g=(3.1g+m)g;(4)根据质量守恒定律可知在17g ZnSO4中含有的SO42-的质量是17g-6.9g=10.1g,则消耗的硫酸的质量是(98÷96)×10.1g=10.3g,所以稀硫酸的溶质质量分数是(10.3g÷60g)×100%=17.2%。
考点:考查实验数据的处理、图像法表示、物质的质量关系及溶液的质量分数的计算的知识。
本题所属考点:【物质的量】
本题难易程度:【一般】
Envy assails the noblest, the winds howl around the highest peak. 峰高招风,位高人妒。 |
|
|