微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
实验题 (14分)某研究性学习小组欲测定室温下(25 ℃、101 kPa)的气体摩尔体积,请回答以下问题。
该小组设计的简易实验装置如图所示:
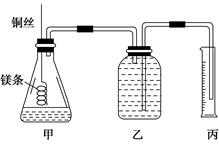
该实验的主要操作步骤如下:
①配制100 mL 1.0 mol/L的盐酸溶液;
②用________(填仪器名称并注明规格)量取7.5mL 1.0 mol/L的盐酸溶液加入锥形瓶中;
③称取a g已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为________;
④往广口瓶中装入足量水,按上图连接好装置,检查装置的气密性;
⑤反应结束后待体系温度恢复到室温,读出量筒中水的体积为V mL。
请将上述步骤补充完整并回答下列问题。
(1)步骤①中,配制100 mL 1.0 mol/L的盐酸溶液时,下列哪些操作会使配制浓度偏小(填写字母)____。
A 用量筒量取浓盐酸时,俯视量筒的刻度 B容量瓶未干燥即用来配制溶液
C浓盐酸在烧杯中稀释时,搅拌时间过长
A.定容完成后,将容量瓶倒置摇匀后,发现液面低于刻度线
E.在容量瓶中定容时俯视容量瓶刻度线 F.烧杯中有少量水
(2)请填写操作步骤中的空格:步骤②_______________ 步骤③___________
(3)实验步骤⑤中应选用__________(填字母)的量筒。
B.100 mL
C.200 mL
D.500 m L
(4)读数时除恢复到室温外,还要注意①______________,②_____________________。
(5)忽略水蒸气影响,在该条件下测得气体摩尔体积的计算式为Vm=____L/mol。
实验题 (14分)某研究性学习小组欲测定室温下(25 ℃、101 kPa)的气体摩尔体积,请回答以下问题。
该小组设计的简易实验装置如图所示:

该实验的主要操作步骤如下:
①配制100 mL 1.0 mol/L的盐酸溶液;
②用________(填仪器名称并注明规格)量取7.5mL 1.0 mol/L的盐酸溶液加入锥形瓶中;
③称取a g已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为________;
④往广口瓶中装入足量水,按上图连接好装置,检查装置的气密性;
⑤反应结束后待体系温度恢复到室温,读出量筒中水的体积为V mL。
请将上述步骤补充完整并回答下列问题。
(1)步骤①中,配制100 mL 1.0 mol/L的盐酸溶液时,下列哪些操作会使配制浓度偏小(填写字母)____。
A 用量筒量取浓盐酸时,俯视量筒的刻度 B容量瓶未干燥即用来配制溶液
C浓盐酸在烧杯中稀释时,搅拌时间过长
A.定容完成后,将容量瓶倒置摇匀后,发现液面低于刻度线
E.在容量瓶中定容时俯视容量瓶刻度线 F.烧杯中有少量水
(2)请填写操作步骤中的空格:步骤②_______________ 步骤③___________
(3)实验步骤⑤中应选用__________(填字母)的量筒。
B.100 mL
C.200 mL
D.500 mL
(4)读数时除恢复到室温外,还要注意①______________,②_____________________。
(5)忽略水蒸气影响,在该条件下测得气体摩尔体积的计算式为Vm=____L/mol。
本题答案:(1)A C (2)②10 mL量筒 ③0.09
本题解析:
试题分析:(1)A.用量筒量取浓盐酸时,俯视量筒的刻度,则浓盐酸的体积偏小,溶质的物质的量偏少,所以配制的溶液的浓度就偏低;正确;B.容量瓶未干燥即用来配制溶液,由于不影响溶质、溶剂的多少,所以对溶液的浓度无影响,错误;C.浓盐酸在烧杯中稀释时,搅拌时间过长,则溶质会挥发,溶质的物质的量偏少,则所配溶液的浓度就偏低,正确;D.定容完成后,将容量瓶倒置摇匀后,发现液面低于刻度线,由于溶液有均一性,所以对溶液的浓度无影响,错误;E.在容量瓶中定容时俯视容量瓶刻度线,则溶液的体积偏小,使所配溶液的浓度就偏高,错误;F.烧杯中有少量水,对溶液的浓度不产生任何影响,错误 www.91exAm.org。(2)填写操作步骤中的空格:步骤②中为了减小误差,应该选择与7.5mL最接近的规格的量筒,用10 mL量筒;步骤③n(HCl)= 1mol/L×0.0075L =0.0075mol,因为Mg与盐酸反应时是按照1:2的物质的量关系反应的,则m(Mg)= (0.0075mol÷2)×24g/mol="0.090g." (3)n(H2)="1/2n(HCl)=" 0.00375mol,若在标准状况下,则V=n・Vm="0." 00375mol×22400ml/mol=84ml,由于室温下温度高于标准状况,所以气体摩尔体积大于22.4L/mol,因此产生的氢气的体积略大于84ml,因此在实验步骤⑤中应选用100 mL量筒,选项是 A。 (4)读数时除恢复到室温外,还要注意①调节量筒高度,使量筒内的液面与集气瓶内的液面相平 ;②读数时眼睛视线应与量筒中水的凹液面相平;(5)在相同的外界条件下,气体的体积等于它排开的液体的体积。忽略水蒸气影响,n(HCl)= 0.00075mol,根据反应方程式:Mg+2HCl=MgCl2+H2↑,则n(H2)="1/2n(HCl)=0." 00375mol,V(H2)=" V" mL,根据n=V÷Vm可得Vm=V÷n=0.001VL÷0.00375mol="V" /3.75="4" V /15 。
考点:考查配制溶液时的误差分析、仪器的选择与使用、气体摩尔体积的计算的知识。
本题所属考点:【物质的量】
本题难易程度:【困难】
Health is better than wealth./ Good health is above wealth. 健康胜过财富。