微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
计算题 (本题共14分)已知:硝酸铜受热易分解。
170℃时,2Cu (NO3)2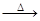 2CuO
2CuO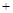 4NO2↑
4NO2↑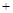 O2↑开始分解,至250℃分解完全。(其中2NO2
O2↑开始分解,至250℃分解完全。(其中2NO2 N2O4,2NO2
N2O4,2NO2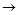 2NO
2NO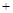 O2等反应忽略不计)。
O2等反应忽略不计)。
800℃时,4CuO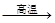 2Cu2O
2Cu2O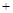 O2↑ 开始分解,至1000℃以上分解完全。
O2↑ 开始分解,至1000℃以上分解完全。
54.取5.64g无水硝酸铜,加热至1000℃以上,将生成的气体导入足量的NaOH溶液充分吸收后,还有逸出的气体是 (填分子式),体积(标准状况)为 ;将吸收液加水稀释到100mL,此溶液中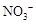 的物质的量浓度为 。
的物质的量浓度为 。
55.取5.64g无水硝酸铜加热至某温度分解后的残留固体中含有1.60g CuO,则残留固体的质量可能是 。
实验证明,当温度达到1800℃时,Cu2O也会发生分解:2Cu2O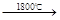 4Cu
4Cu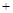 O2↑
O2↑
56.取8.00g CuO,加热到1800℃左右,冷却后称得质量为6.88g,通过计算求出反应后剩余固体中各成分的物质的量之比。
57.取8.00g CuO,通入一定量H2并加热,使其部分还原为Cu和Cu2O,且其中n (Cu2O) n (Cu)
n (Cu)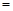 x。将此混合物溶于足量的稀硫酸中(Cu2O
x。将此混合物溶于足量的稀硫酸中(Cu2O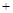 2H
2H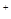
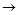 Cu
Cu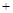 Cu
Cu
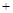 H2O),充分反应后过滤得到Cu y g,试求未被还原的CuO的物质的量(用含x、y的代数式表示)。
H2O),充分反应后过滤得到Cu y g,试求未被还原的CuO的物质的量(用含x、y的代数式表示)。
计算题 (本题共14分)已知:硝酸铜受热易分解。
170℃时,2Cu (NO3)2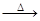 2CuO
2CuO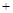 4NO2↑
4NO2↑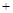 O2↑开始分解,至250℃分解完全。(其中2NO2
O2↑开始分解,至250℃分解完全。(其中2NO2 N2O4,2NO2
N2O4,2NO2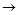 2NO
2NO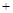 O2等反应忽略不计)。
O2等反应忽略不计)。
800℃时,4CuO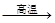 2Cu2O
2Cu2O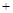 O2↑ 开始分解,至1000℃以上分解完全。
O2↑ 开始分解,至1000℃以上分解完全。
54.取5.64g无水硝酸铜,加热至1000℃以上,将生成的气体导入足量的NaOH溶液充分吸收后,还有逸出的气体是 (填分子式),体积(标准状况)为 ;将吸收液加水稀释到100mL,此溶液中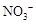 的物质的量浓度为 。
的物质的量浓度为 。
55.取5.64g无水硝酸铜加热至某温度分解后的残留固体中含有1.60g CuO,则残留固体的质量可能是 。
实验证明,当温度达到1800℃时,Cu2O也会发生分解:2Cu2O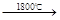 4Cu
4Cu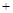 O2↑
O2↑
56.取8.00g CuO,加热到1800℃左右,冷却后称得质量为6.88g,通过计算求出反应后剩余固体中各成分的物质的量之比。
57.取8.00g CuO,通入一定量H2并加热,使其部分还原为Cu和Cu2O,且其中n (Cu2O) n (Cu)
n (Cu)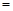 x。将此混合物溶于足量的稀硫酸中(Cu2O
x。将此混合物溶于足量的稀硫酸中(Cu2O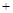 2H
2H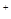
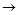 Cu
Cu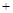 Cu
Cu
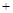 H2O),充分反应后过滤得到Cu y g,试求未被还原的CuO的物质的量(用含x、y的代数式表示)。
H2O),充分反应后过滤得到Cu y g,试求未被还原的CuO的物质的量(用含x、y的代数式表示)。
本题答案:54.O2(1分),0.168L(2分),0.6mol/L(
本题解析:
试题分析:54.取5.64g无水硝酸铜,加热至1000℃以上,发生分解反应:4Cu(NO3)2  2Cu2O+ 8NO2↑+3O2↑,将生成的气体导入足量的NaOH溶液充分吸收后,由于4NO2+O2+2H2O=4HNO3, HNO3+NaOH=NaNO3+ H2O,反应产生的NO2、O2的物质的量的比是8:3,所以根据反应时物质的量的关系可知氧气过量,因此还有逸出的气体是O2;
2Cu2O+ 8NO2↑+3O2↑,将生成的气体导入足量的NaOH溶液充分吸收后,由于4NO2+O2+2H2O=4HNO3, HNO3+NaOH=NaNO3+ H2O,反应产生的NO2、O2的物质的量的比是8:3,所以根据反应时物质的量的关系可知氧气过量,因此还有逸出的气体是O2;
55. n(Cu(NO3)2)=5.64g÷188g/mol=0.03mol,由于加热至某温度分解后的残留固体中含有1.60g CuO,n(CuO)= 1.60g÷80g/mol=0.02mol,根据Cu元素守恒,可能还含有0.01mol的Cu(NO3)2没有分解,则残留固体的质量是0.01mol×188g/mol+1.60g=3.48g;也可能产生的CuO又发生分解反应产生了Cu2O, 根据Cu元素守恒,可能还含有0.005mol的Cu2O,则固体的质量是0.005mol×144g/mol+1.60g=2.32g;
56.n(CuO)= 8.00g÷80g/mol=0.1mol,加热到1800℃左右,若完全转化为Cu2O,则固体的质量是0.1mol÷2×144g/mol=7.2g;若完全转化为Cu,则固体的质量是:0.1mol×64g/mol=6.4g;现在冷却后称得质量为6.4g<6.88g<7.2g,说明在固体中两种成分都含有。假设含有Cu2O、Cu的物质的量分别是x、y;则根据Cu元素守恒可得:2x+y=0.1mol;144x+64y=6.88g。解得x=0.03mol, y=0.04mol,所以n(Cu2O):n(Cu)= 0.03:0.04=3:4。
57.n(CuO)= 8.00g÷80g/mol=0.1mol。假设反应后在混合物中含有Cu2O、Cu、CuO的物质的量分别是a、b、c,则根据Cu元素守恒可得2a+b+c=0.1mol;根据题意可得a/b=x;64(a+b)=y。解得a=xy/64(x+1)mol;b=y/64(x+1)mol;c="0.1―(2a+b)=" nCuO=0.1―(y+2xy)/64(1+x)。
考点:考查物质成分的确定、守恒方法在氧化还原反应方程式计算中的应用的知识。
本题所属考点:【物质的量】
本题难易程度:【困难】
Law makers should not be law breakers. 立法者不可违法。