微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
计算题 (本题共14分)铜有多种化合物,氧化亚铜(Cu2O)、氯化亚铜(CuCl)、氯化铜(CuCl2)、CuSO4等。
完成下列计算:
(1)波尔多液是由硫酸铜、生石灰和水配制成的杀菌剂,不同情况下需要配制不同的比例。现配制按质量比CuSO4:CaO:H2O =1:2:200的波尔多液50Kg。
需要用CuSO4・5H2O g,CaO mol
(2)某工厂以精辉铜矿(主要成分为Cu2S)为原料冶炼金属铜,精辉铜矿中含23%杂质,日均产含Cu量97.5%的粗铜42t。
已知:总反应式 Cu2S+O2 2Cu+SO2
2Cu+SO2
日均需精辉铜矿 t,日均 产SO2标准状况下体积 L
(3)印刷线路板的铜能被FeCl3的溶液腐蚀,将印刷线路板浸入200mL FeCl3溶液中,有11.2gCu被腐蚀掉。取出印刷线路板,向溶液中加入11.2g铁粉,充分反应溶液中还有4.8g不溶物。计算原FeCl3溶液的物质的量浓度。
(4)制备铜的某化合物晶体。取5.12g Cu、14.5mol/L HNO3 15 mL、6.0 mol/L HC1 50mL,混合后Cu完全反应,反应后溶液有中水54.32g,再经水浴保温蒸发掉42g水,冷却至20℃并过滤,得到8.12g晶体。通过计算推断此晶体的化学式 。
已知:20℃溶解度 CuC12・2H2O 73g /100g H2O Cu(NO3)2・3H2O 125g /100g H2O
计算题 (本题共14分)铜有多种化合物,氧化亚铜(Cu2O)、氯化亚铜(CuCl)、氯化铜(CuCl2)、CuSO4等。
完成下列计算:
(1)波尔多液是由硫酸铜、生石灰和水配制成的杀菌剂,不同情况下需要配制不同的比例。现配制按质量比CuSO4:CaO:H2O =1:2:200的波尔多液50Kg。
需要用CuSO4・5H2O &# 160; g,CaO mol
(2)某工厂以精辉铜矿(主要成分为Cu2S)为原料冶炼金属铜,精辉铜矿中含23%杂质,日均产含Cu量97.5%的粗铜42t。
已知:总反应式 Cu2S+O2 2Cu+SO2
2Cu+SO2
日均需精辉铜矿 t,日均产SO2标准状况下体积 L
(3)印刷线路板的铜能被FeCl3的溶液腐蚀,将印刷线路板浸入200mL FeCl3溶液中,有11.2gCu被腐蚀掉。取出印刷线路板,向溶液中加入11.2g铁粉,充分反应溶液中还有4.8g不溶物。计算原FeCl3溶液的物质的量浓度。
(4)制备铜的某化合物晶体。取5.12g Cu、14.5mol/L HNO3 15 mL、6.0 mol/L HC1 50mL,混合后Cu完全反应,反应后溶液有中水54.32g,再经水浴保温蒸发掉42g水,冷却至20℃并过滤,得到8.12g晶体。通过计算推断此晶体的化学式 。
已知:20℃溶解度 CuC12・2H2O 73g /100g H2O Cu(NO3)2・3H2O 125g /100g H2O
本题答案:(本题共14分)
(1)385
本题解析:
试题分析:(1)CuSO4:CaO:H2O =1:2:200的波尔多液50Kg中硫酸铜的质量是50kg×1/(1+2+200)=246.3g,则硫酸铜的物质的量是246.3g/160g/mol,所以需要CuSO4・5H2O的质量是246.3g/160g/mol×250g/mol=385g;CaO的质量是硫酸铜质量的2倍,所以CaO的物质的量是246.3g×2/56g/mol=8.8mol;
(2)日均产含Cu量97.5%的粗铜42t,则Cu的物质的量是42×106g/64g/mol×97.5%=6.4×105mol,根据化学方程式可知需要Cu2S的物质的量是3.2×105mol,所以日均需精辉铜矿的质量是3.2×105mol×160g/mol/(1-23%)=66.5t;日均生成二氧化硫的物质的量也是3.2×105mol,标准状况下的体积是3.2×105mol×22.4L/mol=7.17×106L;
(3)根据题意,剩余不溶物只能是Cu,不可能含有Fe;若存在Fe,则溶液中的铜离子被全部置换出,则不溶物的质量大于11.2g;4.8gCu的物质的量是0.075mol,开始加入Cu的物质的量是11.2g/64g/mol=0.175mol,所以相当于溶解Cu0.1mol,Fe的物质的量是11.2g/56g/mol=0.2mol,则gauge过程中共失去电子的物质的量是(0.2+0.1)mol×2=0.6mol,根据得失电子守恒,则铁离子的物质的量是0.6mol,所以氯化铁溶液的物质的量浓度是0.6mol/0.2L=3.0mol/L;
(4)根据题意,Cu与氢离子、硝酸根离子反应生成铜离子、氮的氧化物、水,氯离子不参加反应,反应前n(HNO3)=0.2175mol,n(HCl)=0.3mol,n(Cu)=5.12g/64g/mol=0.08mol,所以剩余硝酸根量少于氯离子,且Cu(NO3)2・3H2O溶解度大,则析出的是CuC12晶体;无水氯化铜的溶解度是 g;
g;
设晶体化学式为CuC12・xH2O,反应生成氯化铜的质量是0.08mol×135g/mol=10.8g,剩余水的质量是54.32g-42g=12.32g,析出晶体后剩余溶液为氯化铜的饱和溶液,则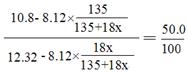 ,解得x=3,该晶体的化学式为CuC12・3H2O。
,解得x=3,该晶体的化学式为CuC12・3H2O。
考点:考查物质化学式的计算,以物质的量为核心的有关计算
本题所属考点:【物质的量】
本题难易程度:【困难】
What colour do you like best?----Red. 你最喜欢的颜色是什么?---红色.