微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 金属钛(Ti)性能优越,被称为继铁、铝之后的“第三金属”。工业上以金红石为原料 制取Ti的反应为
aTiO2 + bCl2+eC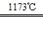 aTiCl4+eCO Ⅰ
aTiCl4+eCO Ⅰ
TiCl4+2Mg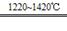 Ti+2MgCl2 Ⅱ
Ti+2MgCl2 Ⅱ
关于反应Ⅰ、Ⅱ的分析不正确的是
①TiCl4在反应Ⅰ中是还原产物,在反应Ⅱ中是氧化剂;②C、Mg在两个反应中均被还原;
③在反应Ⅰ、Ⅱ中Mg的还原性大于C,C的还原性大于TiCl4;
④a=1,b="e" =2 ⑤每生成19.2 g Ti,反应Ⅰ、Ⅱ中共转移4.8 mol e-。
A.①②④ B.②③④ C.③④ D.②③⑤
选择题 金属钛(Ti)性能优越,被称为继铁、铝之后的“第三金属”。工业上以金红石为原料制取Ti的反应为
aTiO2 + bCl2+eC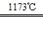 aTiCl4+eCO Ⅰ
aTiCl4+eCO Ⅰ
TiCl4+2Mg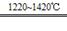 Ti+2MgCl2 Ⅱ
Ti+2MgCl2 Ⅱ
关于反应Ⅰ、Ⅱ的分析不正确的是
①TiCl4在反应Ⅰ中是还原产物,在反应Ⅱ中是氧化剂;②C、Mg在两个反应中均被还原;
③在反应Ⅰ、Ⅱ中Mg的还原性大于C,C的还原性大于TiCl4;
④a=1,b="e" =2 ⑤每生成19.2 g Ti,反应Ⅰ、Ⅱ中共转移4.8 mol e-。
A.①②④ B.②③④ C.③④ D.②③⑤
本题答案:D
本题解析:
试题分析:①aTiO2+bCl2+eC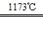 aTiCl4+eCO 该反应中反应前后,碳元素的化合价升高,碳单质作还原剂,氯元素的化合价降低,氯气作氧化剂,还原产物是TiCl4;TiCl4+2Mg
aTiCl4+eCO 该反应中反应前后,碳元素的化合价升高,碳单质作还原剂,氯元素的化合价降低,氯气作氧化剂,还原产物是TiCl4;TiCl4+2Mg Ti+2MgCl2该反应中钛元素的化合价降低,TiCl4作氧化剂;所以TiCl4在反应I中是还原产物,在反应II中是氧化剂,故正确;②C、Mg在反应中反应前后化合价都升高,所以均为还原剂,被氧化,故错误;③在反应I中碳不能还原TiO2,反应II中Mg能还原TiCl4,所以镁的还原性大于C;在反应I中碳作还原剂,TiCl4作还原产物,还原剂 的还原性大于还原产物的还原性,所以C的还原性大于TiCl4,故正确;④根据反应前后各元素的原子个数守恒知,2a=e、2b=4a所以a=1、b=e=2,故正确;⑤将方程式Ⅰ、Ⅱ相加得
Ti+2MgCl2该反应中钛元素的化合价降低,TiCl4作氧化剂;所以TiCl4在反应I中是还原产物,在反应II中是氧化剂,故正确;②C、Mg在反应中反应前后化合价都升高,所以均为还原剂,被氧化,故错误;③在反应I中碳不能还原TiO2,反应II中Mg能还原TiCl4,所以镁的还原性大于C;在反应I中碳作还原剂,TiCl4作还原产物,还原剂 的还原性大于还原产物的还原性,所以C的还原性大于TiCl4,故正确;④根据反应前后各元素的原子个数守恒知,2a=e、2b=4a所以a=1、b=e=2,故正确;⑤将方程式Ⅰ、Ⅱ相加得
TiO2+2Cl2+2C+2Mg=Ti+2CO+2MgCl2 转移电子
48g 8mol
19.2g 3.2mol
所以每生成19.2 g Ti,反应I、II中共转移3.2 mol e-,故错误,故选D。
考点:考查氧化还原反应的有关判断与计算
本题所属考点:【化学基本概念】
本题难易程度:【一般】
All true love is founded on esteem. 真正的爱基于尊重.