微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 二氧化硫和氮的氧化物是大气的主要污染物,防止和治理环境污染是当前环保工作的重要研究内容之一。
(1)一定条件下,2SO2(g)+O2(g)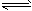 2SO3(g),向2L密闭容器中通入2mol SO2(g)、1mol O2(g)和
2SO3(g),向2L密闭容器中通入2mol SO2(g)、1mol O2(g)和
0.2mol SO3(g),2min后反应达到平衡时,测得SO2的转化率为50%,则该可逆反应的平衡常数K=
_________;恒温下,若往容器中再加入2 mol SO2(g),则重新达到平衡时SO2的总转化率_______50%(选填“>”、“<”或“=”)。
(2)用CH4催化还原NOx为N2可以消除氮氧化物的污染。现有1L NO2、NO混合气体NOx,将其还原成
N2,需同温同压下CH4的体积0.4L,则混合气体中NO2、NO的物质量之比为_________。
(3)新型纳米材料氧缺位铁酸盐(ZnFe2Ox),由铁酸盐(ZnFe2O4)经高温还原制得,常温下,它能使工业废气中的酸性氧化物 分解除去,转化流程如图所示
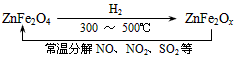
若2mol ZnFe2Ox与SO2可生成0.75 mol S,x=_________。求可分解⑵中混合气体体积V(标准状况下)。(写出计算过程)
填空题 二氧化硫和氮的氧化物是大气的主要污染物,防止和治理环境污染是当前环保工作的重要研究内容之一。
(1)一定条件下,2SO2(g)+O2(g)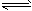 2SO3(g),向2L密闭容器中通入2mol SO2(g)、1mol O2(g)和
2SO3(g),向2L密闭容器中通入2mol SO2(g)、1mol O2(g)和
0.2mol SO3(g),2min后反应达到平衡时,测得SO2的转化率为50%,则该可逆反应的平衡常数K=
_________;恒温下,若往容器中再加入2 mol SO2(g),则重新达到平衡时SO2的总转化率_______50%(选填“>”、“<”或“=”)。
(2)用CH4催化还原NOx为N2可以消除氮氧化物的污染。现有1L NO2、NO混合气体NOx,将其还原成
N2,需同温同压下CH4的体积0.4L,则混合气体中NO2、NO的物质量之比为_________。
(3)新 型纳米材料氧缺位铁酸盐(ZnFe2Ox),由铁酸盐(ZnFe2O4)经高温还原制得,常温下,它能使工业废气中的酸性氧化物分解除去,转化流程如图所示
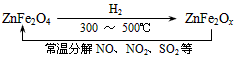
若2mol ZnFe2Ox与SO2可生成0.75 mol S,x=_________。求可分解⑵中混合气体体积V(标准状况下)。(写出计算过程)
本题答案:(1)5.76;<
(2)3∶2
(3)3.25
本题解析:
本题所属考点:【反应速率与平衡的有关计算】
本题难易程度:【一般】
A little neglect may breed great mischief. 细小的疏忽会酿成大祸。