��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
����� ��12�֣��������������ЧӦ����Դ��ȱ����������ӣ���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�������˸������ձ����ӡ�Ŀǰ��ҵ����һ�ַ�������CO2������ȼ�ϼ״���Ϊ̽����Ӧԭ�����ֽ�������ʵ�飬�����Ϊ1 L���ܱ������У�����lmol CO2��3mol H2��һ�������·�����Ӧ��
CO2��g��+3H2(g) 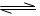 CH3OH(g)+H2O(g) ��H = ��49.0kJ��mo1��
CH3OH(g)+H2O(g) ��H = ��49.0kJ��mo1��
���CO2��CH3OH��g����Ũ����ʱ��仯��ͼ��ʾ��
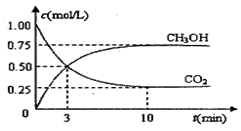
��1���ӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v��H2��=??????????mol/��L��min��
��2���÷�Ӧ��ƽ�ⳣ��Ϊ????????????��
��3�����д�ʩ����ʹn��CH3OH����n��CO2���������??????????��
A�������¶�????????????????B������He��g����ʹ��ϵѹǿ����
C����H2O(g)����ϵ�з���????D���ٳ���lmol CO2��3mol H2
��4����֪�ڳ��³�ѹ�£�
��2CH3OH��1��+3O2��g��=2CO2��g��+4H2O��g����H= ��1275.6kJ/mol
��H2O��g��=H2O��1��?��H= ��44.0kJ/mol
��״���ȼ���Ȼ�ѧ����ʽΪ��??????????????????????????????????��
��5�����ȼ�ռ״�����ɴ�����ѧ����ʧ������Լ״��Ϳ���Ϊԭ�ϣ�����������Ϊ�������Һ��Ƴ�ԭ��ؽ��кܶ��ŵ㣬����д���õ�صĸ�����Ӧ��___________________
��6�������£�ijˮ��ҺM�д��ڵ������У�Na+��A����H+��OH����������ҺM�� pH=3��HA��Һ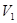 mL��pH=11��NaOH��Һ
mL��pH=11��NaOH��Һ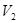 mL��Ϸ�Ӧ���ã�������˵������ȷ����? __��
mL��Ϸ�Ӧ���ã�������˵������ȷ����? __��
A������ҺM�����ԣ�����ҺM�� c��H+��+c��OH����=2��10��7mol��L-1
B����V1=V2������ҺM��pHһ������7
C������ҺM�����ԣ���V1һ������V2
D������ҺM�ʼ��ԣ���V1һ��С��V2
����� ��12�֣��������������ЧӦ����Դ��ȱ����������ӣ���ν��� ������CO2�ĺ�������Ч�ؿ�������CO2�������˸������ձ����ӡ�Ŀǰ��ҵ����һ�ַ�������CO2������ȼ�ϼ״���Ϊ̽����Ӧԭ�����ֽ�������ʵ�飬�����Ϊ1 L���ܱ������У�����lmol CO2��3mol H2��һ�������·�����Ӧ��
CO2��g��+3H2(g) 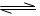 CH3OH(g)+H2O(g) ��H = ��49.0kJ��mo1��
CH3OH(g)+H2O(g) ��H = ��49.0kJ��mo1��
���CO2��CH3OH��g����Ũ����ʱ��仯��ͼ��ʾ��

��1���ӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v��H2��=??????????mol/��L��min��
��2���÷�Ӧ��ƽ�ⳣ��Ϊ????????????��
��3�����д�ʩ����ʹn��CH3OH����n��CO2���������??????????��
A�������¶�????????????????B������He��g����ʹ��ϵѹǿ����
C����H2O(g)����ϵ�з���????D���ٳ���lmol CO2��3mol H2
��4����֪�ڳ��³�ѹ�£�
��2CH3OH��1��+3O2��g��=2CO2��g��+4H2O��g����H= ��1275.6kJ/mol
��H2O��g��=H2O��1��?��H= ��44.0kJ/mol
��״���ȼ���Ȼ�ѧ����ʽΪ��??????????????????????????????????��
��5�����ȼ�ռ״�����ɴ�����ѧ����ʧ������Լ״��Ϳ���Ϊԭ�ϣ�����������Ϊ�������Һ��Ƴ�ԭ��ؽ��кܶ��ŵ㣬����д���õ�صĸ�����Ӧ��___________________
��6�������£�ijˮ��ҺM�д��ڵ������У�Na+��A����H+��OH����������ҺM�� pH=3��HA��Һ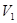 mL��pH=11��NaOH��Һ
mL��pH=11��NaOH��Һ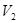 mL��Ϸ�Ӧ���ã�������˵������ȷ����? __��
mL��Ϸ�Ӧ���ã�������˵������ȷ����? __��
A������ҺM�����ԣ�����ҺM��c��H+��+c��OH����=2��10��7mol��L-1
B����V1=V2������ҺM��pHһ������7
C������ҺM�����ԣ���V1һ������V2
D������ҺM�ʼ��ԣ���V1һ��С��V2
����𰸣���1��0.225 ��2�֣�?��2��16/3(5.33) ��2
���������
��v��H2��="3" v��CO2��=(1.0�D0.25)mol/L��3/10min=0.225mol/��L��min��
��?????CO2��g��+3H2(g) 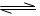 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
Cʼ????? 1??????? 3
C��???? 0.75???? 2.25?????????? 0.75??? 0.75
Cƽ???? 0.25????? 0.75????????? 0.75??? 0.75
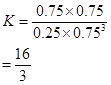
��C? D
A�������¶ȣ�ƽ�������ƶ���n��CH3OH����n��CO2����С��B��ƽ�ⲻ�ƶ���n��CH3OH����n��CO2�����䡣
�ȣ���+4�ڣ�/2�ã�CH3OH(l)+ 3/2 O2 (g) = CO2(g) + 2H2O(L)?��H= -725.8KJ/mol
��5�� CH3OH +8 OH- -6e- = CO32- + 6H2O
��6��AD
�����������㣺����Ӧ������ƽ����йؼ��㡿
�������׳̶ȣ���һ�㡿
Fortune favours the bold. �������ߡ�