微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (10分)一定的温度下向2L密闭容器中通入2molSO2和2molO2,发生反
应: 2SO2+O2 2SO3.5min后达到平衡,测得容器中有SO31.6mol.
2SO3.5min后达到平衡,测得容器中有SO31.6mol.
回答下列问题:
(1)?反应5min内,v(O2)=_________mol.L-1.min-1.
(2)?化学反应达到平衡时,SO2消耗的浓度占起始浓度的百分比为__________;此时,容器中c(O2)=_______,压强是起始时的_______倍.
(3)?判断该反应达到平衡的标志是_______________;
A.v消耗(SO2)=v生成(SO3)
B.混合气体的平均相对分子质量不再改变
C.混合气体的密度不再改变
D.容器中气体的总物质的量不再变化
填空题 (10分)一定的温度下向2L密闭容器中通入2molSO2和2molO2,发生反
应: 2SO2+O2 2SO3.5min后达到平衡,测得容器中有SO31.6mol.
2SO3.5min后达到平衡,测得容器中有SO31.6mol.
回答下列问题:
(1)?反应5min内,v(O2)=_________mol.L-1.min-1.
(2)?化学反应达到平衡时,SO2消耗的浓度占起始浓度的百分比为__________;此时,容器中c(O2)=_______,压强是起始时的_______倍.
(3)?判断该反应达到平衡的 标志是_______________;
A.v消耗(SO2)=v生成(SO3)
B.混合气体的平均相对分子质量不再改变
C.混合气体的密度不再改变
D.容器中气体的总物质的量不再变化
本题答案:(1)0.08?(2)80%;0.6 mol.L-1; 0.
本题解析:(1)考查可逆反应的有关计算。
2SO2??+? O2 2SO3
2SO3
起始量(mol)???????????????????? 2???????? 2????? 0
转化量(mol)??????????????????? 1.6?????? 0.8??? 1.6
平衡量(mol)??????????????????? 0.4?????? 1.2??? 1.6
所以氧气的反应速率是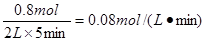
(2)SO2消耗的浓度占起始浓度的百分比为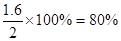
此时氧气的浓度
(3)A中反应速率方向相同,所以不能证明。混合气的密度是混合气的质量和容器容积的比值,质量和容积均不变,所以密度始终是不变的。混合气体的平均相对分子质量是混合气的质量和混合气的物质的量的比值,质量不变,但混合气的物质的量是变化的,所以BD正确,即答案是BD。
本题所属考点:【反应速率与平衡的有关计算】
本题难易程度:【一般】
You should,like a candle,burn yourself out to give light to others. 要象蜡烛一样燃烧自已,照亮别人.