��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
����� ��12�֣�I��һ���¶���,���ݻ�ΪV L���ܱ������н��з�Ӧ��aN��g�� bM��g����M��N�����ʵ�����ʱ��ı仯������ͼ��ʾ��
bM��g����M��N�����ʵ�����ʱ��ı仯������ͼ��ʾ��

��1���˷�Ӧ�Ļ�ѧ����ʽ��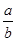 =__________?
=__________?
��2��t1��t2ʱ��,��M��Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ��____________
��3��ƽ��ʱ��N��ת����Ϊ?????????????????????????��
��4��������������˵��������Ӧ�ﵽƽ��״̬����????
A����Ӧ��M��N�����ʵ���֮��Ϊ1�U1
B����� ���������������ʱ��ı仯���仯
C���������������ʵ�������ʱ��ı仯���仯
D����λʱ����ÿ����a mol N��ͬʱ����b mol M
E����������ѹǿ����ʱ��ı仯���仯
F��N�����������ڻ�������б��ֲ���
II����1�����������ǿ����������ɫ��Դ����֪��������ֵ��143kJ��g-1����ȼ��1molH2�ų�������Ϊ???????????????????kJ��
��2��1molN2(g)��1molO2��g����һ�������·�Ӧ����2molNO(g)������180kJ����������֪����1molN2(g)�е�N��N��1molO2��g���е�O=O�ֱ���Ҫ����946kJ��498kJ����������1molNO�����еĻ�ѧ���γ�ʱ���ͷ�_______kJ��������
����� ��12�֣�I��һ���¶���,���ݻ�ΪV L���ܱ������н��з�Ӧ��aN��g�� bM��g����M��N�����ʵ�����ʱ��ı仯������ͼ��ʾ��
bM��g����M��N�����ʵ�����ʱ��ı仯������ͼ��ʾ��

��1���˷�Ӧ�Ļ�ѧ����ʽ��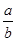 =__________?
=__________?
��2��t1��t2ʱ��,��M��Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ��____________
��3��ƽ��ʱ��N��ת����Ϊ?????????????????????????��
��4��������������˵��������Ӧ�ﵽƽ��״̬����????
A����Ӧ��M��N�����ʵ���֮��Ϊ1�U1
B��������������������ʱ��ı仯���仯
C���������������ʵ�������ʱ��ı仯���仯
D����λʱ����ÿ����a mol N��ͬʱ����b mol M
E����������ѹǿ����ʱ��ı仯���仯
F��N�����������ڻ�������б��ֲ���
II����1�����������ǿ����������ɫ��Դ����֪��������ֵ��143kJ��g-1����ȼ��1molH2�ų�������Ϊ???????????????????kJ��
��2��1molN2(g)��1molO2��g����һ�������·�Ӧ����2molNO(g)������180kJ����������֪����1molN2(g)�е�N��N��1molO2��g���е�O=O�ֱ���Ҫ����946kJ��498kJ����������1molNO�����еĻ�ѧ���γ�ʱ���ͷ�_______kJ��������
����𰸣�I����1��2��2��1/(t2-t1)V? mol��(L��mi
���������I����1������ͼ���֪��Ӧ���е�t1ʱN������8mol��6mol��2mol��M������3mol��2mol��1mol�����ݱ仯��֮������Ӧ�Ļ�ѧ������֮�ȿ�֪a�Ub��2�U1��
��2��t1��t2ʱ��M�����ʵ���������4mo l��3mol��1mol����Ӧ����ͨ���õ�λʱ����Ũ�ȵı仯������ʾ�������M��Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ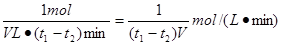 ��
��
��3��ƽ��ʱN�����ʵ���������8mol��2mol��6mol��������ת������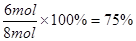 ��
��
��4��M��N�����ʵ���֮��Ϊ1�U1�����ܵó����淴Ӧ�����Ƿ���ȣ�A����˵�������������غ㶨�ɿ�֪������ʼ���Dz���ģ�B����˵������Ϊ��Ӧ�������С�ķ�Ӧ�������ڷ�Ӧ��������������ʵ�����ѹǿ�DZ仯�ģ�ֱ���ﵽƽ��Ų��ٱ仯��C��E����˵����ѡ��D�е����ʷ�������ͬ�ģ���˲���˵����ѡ��F���ڻ�ѧƽ��״̬������������˵����
II����1��1molH2��2g�����Էų���������143kJ��g-1��2g��286kJ��
��2����Ӧ�ȵ��ڶϼ������յ������ͳɼ����ų��������IJ�ֵ����946kJ��498kJ��2��x��180kJ�����x��632kJ��
�����������㣺����Ӧ������ƽ����йؼ��㡿
�������׳̶ȣ���һ�㡿
Fat sorrow is better than lean sorrow. �����г���ǿ�������.