微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (14分) 在温度为373K时,将0.400 mol无色的N2O4气体通入4 L抽空
的密闭容器中,立刻出现红棕色,直至建立N2O4 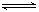 2NO2??的平
2NO2??的平
衡。右图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,
横坐标为时间)(1)该反应的化学平衡常数表达式为K =?????????????。此温度下,K值=??????。
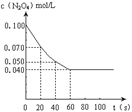
(2)计算在0至20秒时间内,NO2的平均生成速率为????????mol?L-1?s-1。
(3)下表是不同温度下测定得到的该反应的化学平衡常数。
T/ K
| 323
| 373
|
K值
| 0.022
| ?
据此可推测该反应(生成NO2)是???????反应(选填“吸热”或“放热”)。
(4)若其他条件不变,反应在373K时达到平衡后,将N2O4和NO2的浓度都增加至0.4mol/L,平衡将向????????(填“正”或“逆”)反应方向移动。
(5) 反应在373K时达到平衡时,N2O4的转化率=_________________,若将反应容器的容积缩小为原来的一半,则N2O4的转化率将_________(选填“增大”,来源:91考试网“减小”或“不变”)
填空题 (14分) 在温度为373K时,将0.400 mol无色的N2O4气体通入4 L抽空
的密闭容器中,立刻出现红棕色,直至建立N2O4 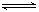 2NO2??的平 2NO2??的平
衡。右图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,
横坐标为时间)(1)该反应的化学平衡常数表达式为K =?????????????。此温度下,K值=??????。

(2)计算在0至20秒时间内,NO2的平均生成速率为????????mol?L-1?s-1。
(3)下表是不同温度下测定得到的该反应的化学平衡常数。
|