微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
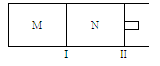
选择题 如图所示,隔板I固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:A(g) + 3B(g)  2C(g)?? ΔH="-192" kJ・mol-1。向M、N中,都通入x mol A和y mol B的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是
2C(g)?? ΔH="-192" kJ・mol-1。向M、N中,都通入x mol A和y mol B的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是
A.若平衡时A气体在两容器中的体积 分数相等,则x一定等于y
B.若x∶y=1∶2,则平衡时,M中的转化率:A>B
C.若x∶y=1∶3,当M中放出热量172.8 kJ时,A的转化率为90%
D.若x=1.2,y=1,N中达到平衡时体积为2 L,含有C 0.4 mol,再通入0.36 mol A时,v(正)<v(逆)
选择题 如图所示,隔板I固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:A(g) + 3B(g)  2C(g)?? ΔH="-192" kJ・mol-1。向M、N中,都通入x mol A和y mol B的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是
2C(g)?? ΔH="-192" kJ・mol-1。向M、N中,都通入x mol A和y mol B的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是

A.若平衡时A气体在两容器中的体积分数相等,则x一定等于y
B.若x∶y=1∶2,则平衡时,M中的转化率:A>B
C.若x∶y=1∶3,当M中放出热量172.8 kJ时,A的转化率为90%
D.若x=1.2,y=1,N中达到平衡时体积为2 L,含有C 0.4 mol,再通入0.36 mol A时,v(正)<v(逆)
本题答案:AD
本题解析:M容器保持恒容,N容器保持恒压,
由于反应前后的气体系数和不等,所以两个平衡态也不一样。要让M、N中平衡时A的体积分数一样,那么只能是M或N中,反应前后不论限度多少,A的体积分数始终为定值。
A(g) + 3B(g)  2C(g)
2C(g)
起始:??? x???? y
反应:??? z???? 3z??????? 2z
平衡:?? x-z??? y-3z?????? 2z
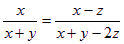 ,则x=y,故A正确;
,则x=y,故A正确;
x∶y=1∶2,即y=2 x,设反应中消耗掉amol A
A(g) + 3B(g)  2C(g)
2C(g)
n(初始)?x???? 2x???????? 0
△n??? a???? 3a???????? 2a
n(平衡) x-a??? 2x-3a?????? 2a
A的转化率=a/x,B的转化率=3a/2x,则平衡时,M中的转化率:A<B,故B错误;
C、题目中热化学方程式的意义:若1mol A完全反应,放热192 kJ,
选项中:x∶y=1∶3,设反应中消耗掉bmol A
即y=3x,A(g) + 3B(g)  2C(g)???放热
2C(g)???放热
n(初始)?x???? 3x???????? 0?????? 192x kJ
△n??? b???? 3b???????? 2b????? 172.8 kJ
即??xmol:192x kJ= b:172.8 kJ,则b="0.9" mol
故A的转化率= b/ x=0.9/ x,C错误;
D、??????????????? A(g) + 3B(g)  2C(g)
2C(g)
n(初始)? 1.2??? 1???????? 0
△n??? 0.2?? 0.6??????? 0.4
n(平衡)?? 1?? 0.4??????? 0.4
则平衡常数K=(0.2 mol/L)2/[0.5 mol/L×(0.2 mol/L)3]=10
原平衡体系中,2.0L容器中含有分子1.0+0.4+0.4=1.8mol,当加入A,体系瞬间有分子1. 8+0.36=2.16mol。N容器恒温、恒压,则容器体积比=气体的物质的量比,
即:2.16/1.8=V/2,瞬间总体积(V)变为2.16×2.00/1.8=2.4L,所以:
Q=(0.4 mol/2.4L)2/[(1.36 mol/2.4L) ×(0.4 mol/2.4L)3]=10.6
Q>K,所以,平衡要逆向移动,即v(正)<v(逆),故D正确;
本题所属考点:【反应速率与平衡的有关计算】
本题难易程度:【一般】
How do you understand misfortune?----Giving in. 你对不幸的理解是什么?---屈服.