微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (共10分)
(1)已知可逆反应:M(g)+N(g)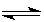 P(g)+Q(g);△H>0,请回答下列问题:
P(g)+Q(g);△H>0,请回答下列问题:
①若要增大M的转化率,在其它条件不变的情况下可以采取的措施为_______________。
A.加入一定量M
B.加入一定量N
C.反应温度升高
D.缩小容器体积
E.加入某物质作催化剂??????? F.分离出一定量P
②在某温度下,反应物的起始浓度分别为:c(M)=" 1" mol・L-1,c(N)="2.4" mol・L-1,达到平衡后,M的转化率为60%,此时N的转化率为_______________。此反应的化学平衡常数K=_______________。
③若反应温度不变,反应物的起始浓度分别为:c(M)=" 4" mol・L-1,c(N)="a" mol・L-1;达到平衡后,c(P)="2" mol・L -1,a=_______________mol・L-1。
(2)随着科学技术的进步,人们研制出了多种类型的甲醇质子交换膜燃料电池,以满足不同的需求。
下图是某笔记本电脑用甲醇质子交换膜燃料电池的结构示意图。甲醇在催化剂作用下提供质子和电子(电子转移的方向如下图所示),电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为:2CH3OH+3O2===2CO2+4H2O。则c电极是?????(填“正极”或“负极”),c电极上发生的电极反应式为_____________________________________________。
填空题 (共10分)
(1)已知可逆反应:M(g)+N(g) P(g)+Q(g);△H>0,请回答下列问题:
P(g)+Q(g);△H>0,请回答下列问题:
①若要增大M的转化率,在其它条件不变的情况下可以采取的措施为_______________。
A.加入一定量M
B.加入一定量N
C.反应温度升高
D.缩小容器体积
E.加入某物质作催化剂??????? F.分离出一定量P
②在某温度下,反应物的起始浓度分别为:c(M)=" 1" mol・L-1,c(N)="2.4" mol・L-1,达到平衡后,M的转化率为60%,此时N的转化率为_______________。此反应的化学平衡常数K=_______________。
③若反应温度不变,反应物的起始浓度分别为:c(M)=" 4" mol・L-1,c(N)="a" mol・L-1;达到平衡后,c(P)="2" mol・L-1,a=_______________mol・L-1。
(2)随着科学技术的进步,人们研制出了多种类型的甲醇质子交换膜燃料电池,以满足不同的需求。
下图是某笔记本电脑用甲醇质子交换膜燃料电池的结构示意图。甲醇在催化剂作用下提供质子和电子(电子转移的方向如下图所示),电子经外电路、质子经内电路到达另一 极与氧气反应,电池总反应为:2CH3OH+3O2===2CO2+4H2O。则c电极是?????(填“正极”或“负极”),c电极上发生的电极反应式为_____________________________________________。
本题答案:(共10分(1)①BCF(各1分,多选倒扣,扣完为止)本题解析:(1)①反应是体积不变的、吸热的可逆反应。所以压强和催化剂不能改变平衡状态,DE不正确。加入一定量M,平衡向正反应方向移动,但M的转化率降低,A不正确。加入一定量N,平衡向正反应方向移动,M的转化率增大,B正确。升高温度平衡向正反应方向移动,M的转化率增大,C正确。分离出一定量P,降低生成物的浓度,平衡向正反应方向移动,M的转化率增大,F正确。所以答案选BCF。
②M的转化率为60%,则消耗M是0.6mol/L。根据反应式可知,消耗N也是0.6mol/L,所以N的转化率是0.6÷2.4×100%=25%。由于同时生成P、Q的浓度也是0.6mol/L,所以平衡常数等于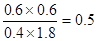 。
。
③达到平衡后,c(P)="2" mol/L,则消耗c(M)="2" mol/L, c(N)="2" mol/L,生成c(Q)="2" mol/L,所以根据平衡常数可知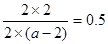 ,记得a=6。
,记得a=6。
(2)c电极是电子流出的,所以是负极。负极甲醇失去电子,电极反应式为CH3OH-6e-+H2O=CO2+6H+。
本题所属考点:【反应速率与平衡的有关计算】
本题难易程度:【一般】
We are all slaves of opinoin. 我们都是意见的奴隶。