��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
����� �����Ϊ1L�����������ܱ������У��ֱ����1molCO��1molH2O(g)�Ļ�����壬�������»�ѧ��Ӧ��CO(g)��H2O(g) CO2(g)��H2(g)����Ӧ��CO�����ʵ����ڲ�ͬ�¶�ʱ���ʵ�����ʱ��ı仯���±���ʾ���ش��������⣺
CO2(g)��H2(g)����Ӧ��CO�����ʵ����ڲ�ͬ�¶�ʱ���ʵ�����ʱ��ı仯���±���ʾ���ش��������⣺
?
| 0min
| 10min
| 20min
| 30min
| 40min
| 50min
|
830��
| 1mol
| 0.8mol
| 0.65mol
| 0.55mol
| 0.5mol
| 0.5mol
|
1100��
| 1mol
| 0.75mol
| 0.6mol
| 0 .6mol
| 0.6mol
| 0.6mol
(1)1100��ʱ��ǰ10min�÷�Ӧ�Ļ�ѧ��Ӧ����v(CO2)=??????????????????��830��ƽ���COת���ʵ�Ϊ__________________��
(2)1100��ʱ��ѧƽ�ⳣ��K��_______���÷�ӦΪ________��Ӧ(����ȡ��͡����ȡ�)��
(3)���жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬��������____________________��
(a)������ѹǿ����?????????? (b)���������c(CO)����
(c)v��(H2)��v��(H2O)????????? (d)c(CO2)��c(CO)
(4)1100��ʱ�ﵽƽ��������������ٳ���2molCO��2molH2O(g)��ƽ��_____________________�ƶ�(ѡ�������Ӧ�������淴Ӧ������)���ٴﵽƽ��ʱ��H2�ٷֺ���________________(ѡ�����С�����䡱)��
(5)830��ʱ���������Ϊ2L���ܱ������г���1molCO2��1molH2�Ļ�����壬60minʱ��Ӧ��ƽ��״̬������c(CO)��c(H2)��ʱ��仯���仯������ͼ��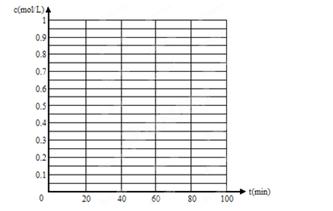
����� �����Ϊ1L�����������ܱ������У��ֱ����1molCO��1molH2O(g)�Ļ�����壬�������»�ѧ��Ӧ��CO(g)��H2O(g) CO2(g)��H2(g)����Ӧ��CO�����ʵ����ڲ�ͬ�¶�ʱ���ʵ�����ʱ��ı仯���±���ʾ���ش��������⣺ CO2(g)��H2(g)����Ӧ��CO�����ʵ����ڲ�ͬ�¶�ʱ���ʵ�����ʱ��ı仯���±���ʾ���ش��������⣺
?
| 0min
| 10min
| 20min
| 30min
| 40min
| 50min
| 830��
| 1mol
| 0.8mol
| 0.65mol
| 0.55mol
| 0.5mol
| 0.5mol
| 1100��
| 1mol
| 0.75mol
| 0.6mol
| 0.6mol
| 0.6mol
| 0.6mol
(1)1100��ʱ��ǰ10min�÷�Ӧ�Ļ�ѧ��Ӧ����v(CO2)=??????????????????��830��ƽ���COת���ʵ�Ϊ__________________��
(2)1100��ʱ��ѧƽ�ⳣ��K��_______���÷�ӦΪ________��Ӧ(����ȡ��͡����ȡ�)��
(3)���жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬��������____________________��
(a)������ѹǿ����?????????? (b)���������c(CO)����
(c)v��(H2)��v��(H2O)????????? (d)c(CO2)��c(CO)
(4)1100��ʱ�ﵽƽ��������������ٳ���2molCO��2molH2O(g)��ƽ��_________��Դ:91������____________�ƶ�(ѡ�������Ӧ�������淴Ӧ������)���ٴﵽƽ��ʱ��H2�ٷֺ���________________(ѡ�����С�����䡱)��
(5)830��ʱ���������Ϊ2L���ܱ������г���1molCO2��1molH2�Ļ�����壬60minʱ��Ӧ��ƽ��״̬������c(CO)��c(H2)��ʱ��仯���仯������ͼ��
����𰸣���1��0.025mol/(L��min) ��1�֣�?? 50%
���������(1)1100��ʱ��ǰ10min��CO�����ʵ���������0.25mol����������CO2ʱ0.25mol����CO2�ķ�Ӧ������0.25mol��1L��10min��0.025mol/(L��min) ��830��ƽ���ʣ��CO��0.5mol�����ԣ�����CO��0.5mol�����ת������0.5��1��100����50����
��2��1100��ƽ��ʱCO(g)��H2O(g)��CO2(g)��H2(g)���ʵ����ֱ���0.6mol��0.6mol��0.4mol��0.4mol������ƽ�ⳣ����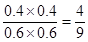 ���¶�Խ��ƽ��ʱCO�����ʵ���Խ��˵�������¶�ƽ�����淴Ӧ�����ƶ�����������Ӧ�Ƿ��ȷ�Ӧ�� ���¶�Խ��ƽ��ʱCO�����ʵ���Խ��˵�������¶�ƽ�����淴Ӧ�����ƶ�����������Ӧ�Ƿ��ȷ�Ӧ��
��3����һ�������£������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ������Ϊ0�����������ʵ�Ũ�Ȼ��������ٷ����仯��״̬���ǻ�ѧƽ��״̬������b��ȷ��ƽ��ʱŨ�Ȳ��ٷ����仯��������֮���Ũ�Ȳ�һ����Ȼ�����ij�ֹ�ϵ��d����ȷ����Ӧǰ��������䣬����ѹǿʼ���Dz���ģ�a����ȷ��C�з�Ӧ���ʵķ����෴������������֮������Ӧ�Ļ�ѧ������֮�ȣ���ȷ�����Դ�ѡbc��
��4������Ӧ���Ũ�ȣ�ƽ��������Ӧ�����ƶ��������ڷ�Ӧǰ���������ģ���CO��ˮ���������ʵ���֮�Ȼ���1�U1�ģ�����ƽ���ǵ�Ч�ģ���������ĺ������䡣
��5�����ڷ�Ӧǰ��������䣬��ƽ���ǵ�Ч�ģ���ƽ��ʱ�������ʵ�Ũ�Ⱦ����룬����ͼ��Ϊ�����𰸣���
�����������㣺����Ӧ������ƽ����йؼ��㡿
�������׳̶ȣ���һ�㡿
Wisdom comes form extensive observation and broad knowledge. ���������ڼ���ʶ��. |
|