微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
计算题 (10分).已知一氧化碳与水蒸气的反应为CO+H2O CO2+H2;在827℃时的平衡常数是100,如果反应开始时,一氧化 碳和水蒸气的浓度都是0.011mol/L,计算:一氧化碳在此反应条件下的平衡转化率。
CO2+H2;在827℃时的平衡常数是100,如果反应开始时,一氧化 碳和水蒸气的浓度都是0.011mol/L,计算:一氧化碳在此反应条件下的平衡转化率。
计算题 (10分).已知一氧化碳与水蒸气的反应为CO+H2O CO2+H2;在827℃时的平衡常数是100,如果反应开始时,一氧化碳和水蒸气的浓度都是0.011mol/L,计算:一氧化碳在此反应条件下的平衡转化率。
CO2+H2;在827℃时的平衡常数是100,如果反应开始时,一氧化碳和水蒸气的浓度都是0.011mol/L,计算:一氧化碳在此反应条件下的平衡转化率。
本题答案:9.09%
本题解析:
试题分析:???????? CO????+ ??H2O???=?? CO2???+?? H2
起始浓度(mol/l)?? 0.011????? 0.011???????? 0??????? 0
转化浓度(mol/l)??? x????????? x??????????? x??????? x
平衡浓度(mol/l)0.011-x ??0.011-x????????x???????x
因为
所以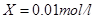
因此转化率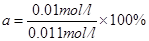 =9.09%
=9.09%
点评:在进行可逆反应的有关计算时,一般采用“三段式”进行,即分别列出起始量、转化量和平衡量或某深刻的量,然后依据已知条件列式计算即可。
本题所属考点:【反应速率与平衡的有关计算】
本题难易程度:【一般】
Art lies in concealing art. 艺术在于使人看不见艺术。