微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题来源:www.91exam.org (14分)在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g)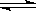 CO(g)+H2O(g),
CO(g)+H2O(g),
其化学平衡常数K和温度t的关系如下表:
t℃
| 700
| 800
| 830
| 1000
| 1200
|
K
| 0.6
| 0.9
| 1.0
| 1.7
| 2.6
回答下列问题:
(1)该反应的化学平衡常数表达式为K=?????????????。
(2)该反应为??????反应(选填吸热、放热)。
(3)能判断该反应是否达到化学平衡状态的依据是??????
(a)容器中压强不变????????(b)混合气体中 c(CO)不变
(c)v正(H2)=v逆(H2O)???(d)c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式: c(CO2)・c(H2)=c(CO)・c(H2O),试判断此时的温度为??????℃。
填空题 (14分)在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g)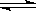 CO(g)+H2O(g), CO(g)+H2O(g),
其化学平衡常数K和温度t的关系如下表:
t℃
| 700
| 800
| 830
| 1000
| 1200
| K
| 0.6
| 0.9
| 1.0
| 1.7
| 2.6
回答下列问题:
(1)该反应的化学平衡常数表达式为K=?????????????。
(2)该反应为??????反应(选填吸热、放热)。
(3)能判断该反应是否达到化学平衡状态的依据是??????
(a)容器中压强不变????????(b)混合气体中 c(CO)不变
(c)v正(H2)=v逆(H2O)???(d)c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式: c(CO2)・c(H2)=c(CO)・c(H2O),试判断此时的温度为??????℃。
本题答案:(共14分)(1)化学平衡常数是在 一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值。所以根据反应的化学方程式可知,该反应的平衡常数表达式是K=<img onload='if(this.width>600)makesmallpic(this,600,1800);' src=) 。 。
(2)根据表中数据可知,随着温度的升高,平衡常数逐渐增大。这说明升高温度,平衡向正反应方向移动,因此正反应是吸热反应。
(3)在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,所以选项b之前;根据方程式可知,反应前后体积不变,所以压强始终是不变的,a不正确;c中反应速率的方向相反,且满足速率之比是相应的化学计量数之比,正确;平衡时各种物质的浓度不再发生变化,但各种物质的浓度之间不一定相等或满足某种关系,d不正确,答案选bc。
(4)将c(CO2)・c(H2)=c(CO)・c(H2O)代入平衡常数表达式可知,K=1,所以温度是830℃。
点评:平衡常数的大小可以衡量反应的进行的程度,该常数只与温度和化学计量数有关系。在平衡状态的判断、可逆反应的有关计算中,平衡常数都起着非常重要的作用,需要熟练掌握,并能灵活运用。
本题所属考点:【反应速率与平衡的有关计算】
本题难易程度:【一般】
Cloudy mornings turn to clear evenings. 早见云雾晚见晴。 |
|