微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (12分)已知可逆反应CO + H2O (g) CO2 + H2,在830K温度下达到平衡。
CO2 + H2,在830K温度下达到平衡。
(1)其化学平衡常数K的表达式为K=??????????????。
(2)830K时,若起始时:c (CO) = 2 mol/L,c (H2O) = 3 mol/L,平衡时CO的转化率为60%,水蒸气的转化率为______________;K值为______________。
(3)830K,若只将起始时c (H2O)改为6 mol/L,则水蒸气的转化率为____________。
(4)若830K时,起始浓度c (CO)=a mol/L,c (H2O)=b mol/L,H2的平衡浓度c (H2)=c mol/L,
①a、b、c之间的关系式是____________________________________;
②当a = b时,a= ________c。
填空题 (12分)已知可逆反应CO + H2O (g) CO2 + H2,在830K温度下达到平衡。
CO2 + H2,在830K温度下达到平衡。
(1)其化学平衡常数K的表达式为K=??????????????。
(2)830K时,若起始时:c (CO) = 2 mol/L,c (H2O) = 3 mol/L,平衡时CO的转化率为60%,水蒸气的转化率为______________;K值为______________。
(3)830K,若只将起始时c (H2O)改为6 mol/L,则水蒸气的转化率为____________。
(4)若830K时,起始浓度c (CO)=a mol/L,c (H2O)=b mol/L,H2的平衡浓度c (H2)=c mol/L,
①a、b、c之间的关系式是________________________________ ____;
②当a = b时,a= ________c。
本题答案:(1)K=化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以根据反应的化学方程式可知,该反应的平衡常数表达式K=<img onload='if(this.width>600)makesmallpic(this,600,1800);' src=) 。
。
(2)??????????????? CO + H2O (g) CO2 + H2
CO2 + H2
起始浓度(mol/L)??? 2???? 3????????? 0??? 0
转化浓度(mol/L)??? 1.2?? 1.2??????? 1.2? 1.2
平衡浓度(mol/L)??? 0.8?? 1.8??????? 1.2? 1.2
所以平衡时水蒸气的转化率为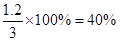
平衡常数K=
(3)??????????????? CO + H2O (g) CO2 + H2
CO2 + H2
起始浓度(mol/L)??? 2???? 6????????? 0??? 0
转化浓度(mol/L)??? x???? x????????? x??? x
平衡浓度(mol/L) (2-x)(6-x)???? x??? x
所以K=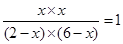
解得x=1.5mol/L
所以水蒸气的转化率是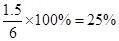
(4)①????????????? CO + H2O (g) CO2 + H2
CO2 + H2
起始浓度(mol/L)??? a???? b????????? 0??? 0
转化浓度(mol/L)??? c???? c????????? c??? c
平衡浓度(mol/L) (a-c)? (b-c)??????? c??? c
所以根据平衡常数的表达式可知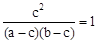
②根据①中关系式可知,当a = b时,a=2c
点评:该题是高考中的常见题型,属于中等难度的试题,试题贴近高考,注重基础和能力的双向考查,有利于培养学生分析问题、解决问题的能力。该题难易适中,学生不难得分。
本题所属考点:【反应速率与平衡的有关计算】
本题难易程度:【一般】
Give credit where credit is due. 有功则赏。