微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (10分)甲醇是一种可再生能源,具有广泛的开发和应用前景。请回答:
(1)工业上合成甲醇CO(g) + 2H2(g)? ??CH3OH(g)? ΔH,在不同温度下的化学平衡常数(K)如表所示。
??CH3OH(g)? ΔH,在不同温度下的化学平衡常数(K)如表所示。
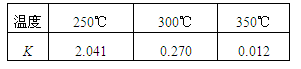
①根据表中数据可判断ΔH??????(填“>” 或 “=” 或 “<”)0。?????
②300℃时,向容积为1L的密闭容器中充入2 mol CO、3 mol H2和2 mol CH3OH,此时反应将???????????????。
A.向正方向移动???????B.向逆方向移动???????C.处于平衡状态??
(2)已知在常温常压下:
①2CH3OH(l) + 3O2(g ) = 2CO2(g) + 4H2O(l)?? ΔH= -a? kJ・mol-1
②2CO (g)+ O2(g) = 2CO2(g)??ΔH= -b kJ・mol-1
写出该条件下甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
???????????????????????????????????????????????????????。
(3)改变下列条件,能同时加快正反应的速率,增大CO的转化率的是?????????
A.使用催化剂????????????B.缩小容器体积
C.降低温度??????????????D.分离CH3OH的物质的量
(4)以甲醇、氧气为原料,KOH溶液作为电解质溶液构成燃料电池总反应为:2CH3OH +3O2+4OH- = 2CO32- + 6H2O,则负极的电极反应式为?????????????????。
填空题 (10分)甲醇是一种可再生能源,具有广泛的开发和应用前景。请回答:
(1)工业上合成甲醇CO(g) + 2H2(g)? ??CH3OH(g)? ΔH,在不同温度下的化学平衡常数(K)如表所示。
??CH3OH(g)? ΔH,在不同温度下的化学平衡常数(K)如表所示。

①根据表中数据可判断ΔH??????(填“>” 或 “=” 或 “<”)0。?????
②300℃时,向容积为1L的密闭容器中充入2 mol CO、3 mol H2和2 mol CH3OH,此时反应将???????????????。
A.向正方向移动???????B.向逆方向移动???????C.处于平衡状态??
(2)已知在常温常压下:
①2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(l)?? ΔH= -a? kJ・mol-1
②2CO (g)+ O2(g) = 2CO2(g)??ΔH= -b kJ・mol-1
写出该条件下甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
???????????????????????????????????????????????????????。
(3)改变下列条件,能同时加快正反应的速率,增大CO的转化率的是?????????
A.使用催化剂????????????B.缩小容器体积
C.降低温度??????????????D.分离CH3OH的物质 91exam .org的量
(4)以甲醇、氧气为原料,KOH溶液作为电解质溶液构成燃料电池总反应为:2CH3OH +3O2+4OH- = 2CO32- + 6H2O,则负极的电极反应式为?????????????????。
本题答案:(10分)(1)①<????②A
(2)CH3OH(l
本题解析:
试题分析:(1)随着温度的升高,平衡常数逐渐减小。这说明升高温度,破坏向逆反应方向移动,所以正方应是放热反应,即△H小于0。
(2)根据盖斯定律可知(①-②)÷2即得到反应CH3OH(l) + O2(g) = CO(g) + 2H2O(l),所以该反应的反应热△H= -(a―b)/2? kJ・mol-1。
(3)催化剂并能改变平衡状态,A不正确;缩小容器体积,增大压强,反应速率加快,平衡向正反应方向移动,增大CO的转化率,B正确;降低温度,反应速率降低,C不正确;分离CH3OH的物质的量,反应速率也是降低的,不正确,答案选B。
(4)根据反应式可知,甲醇失去电子,在负极通入,所以负极的电极反应式是CH3OH-6 e- + 8OH― = CO32― + 6 H2O。
点评:该题是中等难度的试题,也是高考中的常见题型。该题综合性强,难易适中,侧重对学生能力的培养和解题方法的指导与训练。有助于培养学生的逻辑思维能力和发散思维能力,提高学生灵活运用基础知识解决实际问题的能力。该题的关键是明确原电池的工作原理,以及外界条件对平衡状态的影响,然后结合题意灵活运用即可。
本题所属考点:【反应速率与平衡的有关计算】
本题难易程度:【一般】
Virtue is beyond price./ Virtue is a jewel of great price. 美德乃无价之宝.