微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
计算题 在某温度下,将H2和I2各0.10mol 的气态混合物充入10L的密闭容器中,充分反应,达到平衡后,测得 c(H2)= 0.0080mol/L
(1)求该反应的平衡常数。
(2)在上述温度下,该容器中若通入H2和I2各 0.20mol 的气态混合物,试求达到化学平衡状态时各物质的物质的量浓度。
计算题 在某温度下,将H2和I2各0.10mol 的气态混合物充入10L的密闭容器中,充分反应,达到平衡后,测得 c(H2)= 0.0080mol/L
(1)求该反应的平衡常数。
(2)在上述温度下,该容器中若通入H2和I2各0.20mol 的气态混合物,试求达到化学平衡状态时各物质的物质的量浓度。
本题答案:(14分)?(1)K = 0.25(5分)
(2)(各
本题解析:
试题分析:???????????? H2??+?? I2 2HI
2HI
起始浓度(mol/L)???? 0.01???? 0.01?? 0
转化浓度(mol/L)?? 0.002?? 0.002?? 0.004
平衡浓度(mol/L)? 0.008??? 0.008?? 0.004
所以该反应的平衡常数K=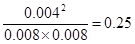
H2??+?? I2 2HI
2HI
起始浓度(mol/L)???? 0.02???? 0.02?? 0
转化浓度(mol/L)???? x???????? x???? x
平衡浓度(mol/L)? 0.02-x?? 0.02-x?? 2x
所以根据反应的平衡常数K可知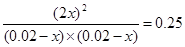
解得x=0.004mol/L
则平衡时c(H2)=0.016mol/L
c(I2)=0.016mol/L
c(HI)=0.0080mol/L
点评:在进行可逆反应的有关计算时,一般采用“三段式”进行,即分别列出起始量、转化量和平衡量或某深刻的量,然后依据已知条件列式计算即可。有利于培养学生的逻辑推理能力和规范答题能力。
本题所属考点:【反应速率与平衡的有关计算】
本题难易程度:【一般】
You eat and eat, but you do not drink to fill you. 吃饭要饱,饮酒要少。