微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
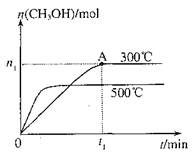
选择题 在容积为2L的密闭容器中进行反应:CO(g)+2H2(g) CH3OH(g),其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图,下列说法正确的是
CH3OH(g),其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图,下列说法正确的是
A.该反应的△H<0
B.其他条件不变,升高温度反应的平衡常数 增大
C.300℃时,0–t1 min内CH3OH的平均生成速率为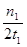 mol?L-1 min-1
mol?L-1 min-1
D.A点的反应体系从300℃升高到500℃,达到平衡时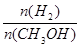 减小
减小
选择题 在容积为2L的密闭容器中进行反应:CO(g)+2H2(g) CH3OH(g),其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图,下列说法正确的是
CH3OH(g),其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图,下列说法正确的是

A.该反应的△H<0
B.其他条件不变,升高温 度反应的平衡常数增大
C.300℃时,0–t1 min内CH3OH的平均生成速率为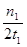 mol?L-1 min-1
mol?L-1 min-1
D.A点的反应体系从300℃升高到500℃,达到平衡时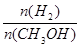 减小
减小
本题答案:AC
本题解析:
试题分析:读图,300℃变为500℃,平衡时甲醇的物质的量减小,说明平衡向逆反应方向移动,由于升高温度时平衡向吸热方向移动,则逆反应是吸热反应,因此推断正反应是放热反应,正反应的焓变小于0,故A正确;平衡常数是生成物平衡浓度幂之积与反应物平衡浓度幂之积的比值,升高温度平衡向逆反应方向移动,则生成物浓度减小、反应物浓度增大,因此推断升高温度时反应的平衡常数减小,故B错误;根据平均反应速率的定义式直接计算,v(CH3OH)=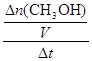 =
=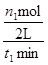 =
=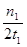 mol/(L?min),故C正确;A点的反应体系为300℃的平衡体系,因为正反应是放热反应,从300℃升高到500℃,平衡向逆反应方向移动,氢气的物质的量增大,甲醇的物质的量减小,则达到平衡时
mol/(L?min),故C正确;A点的反应体系为300℃的平衡体系,因为正反应是放热反应,从300℃升高到500℃,平衡向逆反应方向移动,氢气的物质的量增大,甲醇的物质的量减小,则达到平衡时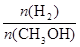 的值增大,故D错误。
的值增大,故D错误。
本题所属考点:【反应速率与平衡的有关计算】
本题难易程度:【简单】
A full belly neither fights nor flies well. 肚子太饱,不能打仗也不能逃跑。