微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
计算题 在一密闭容器中发生反应: 2A(g)+B(g) E(g)
E(g)
(1)写出该反应的平衡常数表达式___________???????____,已知升高温度时,v(正)>v(逆),此时K值__?????__(填“变大”“变小”或“不变”);该反应的△H_____0(填“>”、“=”、“<”);
(2)将1.0mol A和1.0mol B混合后装入2L容器中发生反应,E的物质的量的变化如图所示。
①3分钟内E的平均反应速率为________? ??????_________;
②求此温度下该反应的平衡常数K=?????????????????(结果保留小数后1位);
③请在图中画出5分钟内A的物质的量变化的曲线;
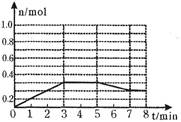
(3)已知在如图所示的变化中,平衡常数K保持不变,则在5~7min内引起E的物质的量变化的原因可能是____________(填编号)。
①降低了温度?②升高了温度?③使用了催化剂?④增大了容器的体积?⑤缩小了容器的体积?⑥减少了A的物质的量。
计算题 在一密闭容器中发生反应: 2A(g)+B(g) E(g)
E(g)
(1)写出该反应的平衡常数表达式___________???????____,已知升高温度时,v(正)>v(逆),此时K值__?????__(填“变大”“变小”或“不变”);该反应的△H_____0(填“>”、“=”、“<”);
(2)将1.0mol A和1.0mol B混合后装入2L容器中发生反应,E的物质的量的变化如图所示。
①3分钟内E的平均反应速率为________???????_________;
②求此温度下该反应的平衡常数K=?????????????????(结果保留小数后1位);
③请在图中画出5分钟内A的物质的量变化的曲线;

(3)已知在如图所示的变化中,平衡常数K保持不变,则在5~7min内引起E的物质的量变化的原因可能是____________(填编号)。
①降低了温度?②升高了温度?③使用了催化剂?④增大了容器的体积?⑤缩小了容器的体积?⑥减少了A的物质的量。
本题答案:(14分)(1)由于化学平衡常数等于生成物浓度幂之积与反应物浓度幂之积的比值,则该反应的平衡常数为c(E)/[c2(A)・c(B)];根据化学平衡移动原理可知,平衡时升高温度,v(正)>v(逆),前者导致平衡向吸热反应方向移动,后者导致平衡向正反应方向移动,则正反应是吸热反应;升高温度导致平衡向正反应方向移动时,生成物浓度增大、反应物浓度减小,根据化学平衡常数的计算式可知,则该反应的平衡常数变大或增大;(2)①读图可知,3分钟内E由0增加到0.3mol,根据平均反应速率的计算式(v=△c/△t=△n/(V・△t)),则v(E)=0.3mol/(2L×3min)=0.050mol/(L・min);②解:依题意,该反应各组分起始、变化、平衡的浓度均已知,则:<br> 2A(g)? +? B(g) <img onload='if(this.width>600)makesmallpic(this,600,1800);' src=) ?E(g)
?E(g)
起始浓度/ mol?Lˉ1?????????????? 0.5?????? 0.5??????? 0
变化浓度/ mol?Lˉ1?????????? ????0.3?????? 0.15????? 0.15
平衡浓度/ mol?Lˉ1?????????????? 0.2?????? 0.35????? 0.15
K= c(E)/[c2(A)・c(B)]=" 0.15/[" 0.22×0.35]≈10.7
答:此温度下该反应的平衡常数K为10.7。
③画图要点:a.依题意,起点(或t=0)时,A为1.0mol;b.未达平衡时,A逐渐减小;c.拐点(或平衡点、t=3min),n(A)="c(A)" ?V=0.2mol?Lˉ1×2L=0.4mol;d.t=3min~5min时,该反应处于化学平衡状态,A为0.4mol,保持不变。
(3)平衡常数只与温度有关,由于正反应是吸热反应,降低温度平衡左移,生成物浓度减小、反应物浓度增大,则c(E)/[c2(A)・c(B)]的比值减小,所以平衡常数K减小,故①错误;升高温度平衡右移,生成物浓度增大、反应物浓度减小,则c(E)/[c2(A)・c(B)]的比值增大,所以平衡常数K增大,故②错误;使用催化剂时,平衡不移动,E的物质的量不减小,平衡常数K也不变,故③错误;增大容器体积,各组分浓度均减小,实质就是减小压强,由于正反应是气态物质体积减小的反应,减小压强平衡左移,则E的物质的量减小,但平衡常数K不变,故④正确;缩小容器体积,各组分浓度均增大,实质就是增大压强,平衡右移,则E的物质的量增大,但平衡常数K不变,故⑤错误;减小A的物质的量,就是减小反应物浓度,平衡左移,则E的物质的量减小,但平衡常数K不变,故⑥正确。
本题所属考点:【反应速率与平衡的有关计算】
本题难易程度:【简单】
A still tongue makes a wise head. 沉默者有智慧。