��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
����� �⼰�仯�����������������о��й㷺����;������������Ԫ���йص����⣺
��1�����������е���Ԫ��֮һ����һ������Ԫ�ء������ƹ㡰�ӵ�ʳ�Ρ�������һ��������KIO3��������KI����ԭ����???????????????????????????????��
��2�������£�NH4I��һ�ֹ��壬һ���¶������ܱ������з�������ķ�Ӧ��
�� NH4I(s) 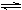 ?NH3(g)? + HI(g)
?NH3(g)? + HI(g)
�� 2HI(g) 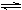 ?H2(g) + I2(g)
?H2(g) + I2(g)
�ﵽƽ��ʱ����С���������������ϵѹǿ������������ɫ????????��������dz�����䡱�����ﵽƽ��ʱ����Ӧ�ڵĻ�ѧƽ�ⳣ������ʽΪ ???????????���ﵽƽ��ʱc(H2)=0.5mol/L����Ӧ�ٵĻ�ѧƽ�ⳣ��Ϊ20���� c (HI) = ???????????????��
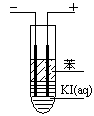
��3����ͼ���ڴ��Թ��м��뱥�͵�KI��Һ��Ȼ���ټ��뱽����������ʯī�缫����ֱͨ����Դ�����ӵ�Դ�����ĵ缫Ϊ?????�����缫��ӦʽΪ?????????????????��ͨ��һ��ʱ��Ͽ���Դ�����Թܣ��ϲ���ҺΪ??????ɫ��
��4����֪Ksp(PbI2)��7.1��10-9mol3/L3����ʢ�г����PbI2������Һ���Թ��У��μ�Ũ��Ϊ0.1mol/L�ĵ⻯����Һ�������Թ۲쵽��Һ���л�ɫ���Dz�������Щ��ɫ���ǵijɷ���??????????��
����� �⼰�仯�����������������о��й㷺����;������������Ԫ���йص����⣺
��1�����������е���Ԫ��֮һ����һ������Ԫ�ء������ƹ㡰�ӵ�ʳ�Ρ�������һ��������KIO3��������KI����ԭ����???????????????????????????????��
��2�������£�NH4I��һ�ֹ��壬һ���¶������ܱ������з�������ķ�Ӧ��
�� NH4I(s) 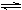 ?NH3(g)? + HI(g)
?NH3(g)? + HI(g)
�� 2HI(g) 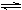 ?H2(g) + I2(g)
?H2(g) + I2(g)
�ﵽƽ��ʱ����С���������������ϵѹǿ������������ɫ????????��������dz�����䡱�����ﵽƽ��ʱ����Ӧ�ڵĻ�ѧƽ�ⳣ������ʽΪ???????????���ﵽƽ��ʱc(H2)=0.5mol/L����Ӧ�ٵĻ�ѧƽ�ⳣ��Ϊ20���� c (HI) = ???????????????��
��3����ͼ���ڴ��Թ��м��뱥�͵�KI��Һ��Ȼ���ټ��뱽����������ʯī�缫����ֱͨ����Դ�����ӵ�Դ�����ĵ缫Ϊ?????�����缫��ӦʽΪ?????????????????��ͨ��һ��ʱ��Ͽ���Դ�����Թܣ��ϲ���ҺΪ??????ɫ��

��4����֪Ksp(PbI2)��7.1��10-9mol3/L3����ʢ�г����PbI2������Һ���Թ��У��μ�Ũ��Ϊ0.1mol/L�ĵ⻯����Һ�������Թ۲쵽��Һ���л�ɫ���Dz�������Щ��ɫ���ǵijɷ���???????? ??��
����𰸣�
��1��KI�ڿ��������ױ�������������KIO3�Ƚ��ȶ�
���������
�����������1��KI�ڿ��������ױ������������ʣ������к����ʣ���KIO3�Ƚ��ȶ�����2���ﵽƽ��ʱ����
С���������������ϵѹǿ������������ɫ�϶��DZ���ġ���Ӧ�ٵ�ƽ�ⳣ��k=c��NH3��?c��HI����
��Ӧ�ڵ�ƽ�ⳣ��k=c(H2)��c(I2)/ c2 (HI)?���ɷ�Ӧ�ڿ�֪�ֽ��c��HI��Ϊƽ��ʱc��H2����
2����ƽ��ʱc��HI��=xmol?L-1�����������ʵ���Ũ��Ϊ��c��NH3��=��x+1)mol?L-1��
���뷴Ӧ�ٵ�ƽ�ⳣ��k=c��NH3��?c��HI��=��x+1)��x=20���㣬�õ�ƽ��ʱc��HI��=4mol?L-1��
���Դ����������Ϊ������������H+�ŵ磬? 2H2O + 2e�� = 2OH�� + H2����������������
I-�ŵ磺2I- -2e�� =I2 ���ϲ������е�ı��㣬���Ϻ�ɫ����4��Ksp(PbI2)��c��Pb2+��c��I-��2?= 7.1��10-9mol3/L3��c��Pb2+��=1.53��10-3mol/L��c��I-��=2.06��10-3mol/L���μ�Ũ��Ϊ0.1mol/L�ĵ⻯����Һ�������Թ۲쵽��Һ���л�ɫPbI2���Dz�����
�����������㣺����Ӧ������ƽ����йؼ��㡿
�������׳̶ȣ������ѡ�
Overeating will cause indigestion. ̰�������.