微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 &n bsp;(12分)向体积为2L的固定密闭容器中通入3molX气体,在一定温度下发生如下反应:
2X(g) Y(g)+3Z(g)
Y(g)+3Z(g)
(1)经5min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y的物质的量浓度变化表示的速率为?????????????。
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一段时间内测得容器内的反应速率分别为:甲v(X)=3.5mol/(L?min);乙v(Y)=2mol/(L?min);丙v(Z)=4.5mol/(L?min);丁v(X)=0.075mol/(L?s)。若其它条件相同,温度不同,则温度由高到低的顺序是(填序号) ???????????。
(3)若向达到(1)的平衡体系中充入氩气,则平衡向 ????????????(填"左"或"右"或"不")移动;若向
达到(1)的平衡体系中移走部分混合气体,则平衡向 ?????????(填" 左 " 或 " 右 " 或 " 不")移动。
(4)若在相同条件下向达到(1)所述的平衡体系中再充入0.5molX气体,则平衡后X的转化率⑷与⑴的
平衡中的X的转化率相比较??????????????。
A.无法确定
B.⑷一定大于⑴
C.⑷一定等于⑴
D.⑷一定小于⑴
(5)若保持温度和压强不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,达到平衡时仍
与(1)的平衡等效,则a、b、c应该满足的关系为 ???????????????????????。
(6)若保持温度和体积不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,达到平衡时仍
与(1)的平衡等效,且起始时维持化学反应向逆反应方向进行,则c的取值范围应该为 ?????????????。
填空题 (12分)向体积为2L的固定密闭容器中通入3molX气体,在一定温度下发生如下反应:
2X(g) Y(g)+3Z(g)
Y(g)+3Z(g)
(1)经5min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y的物质的量浓度变化表示的速率为?????????????。
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一段时间内测得容器内的反应速率分别为:甲v(X)=3.5mol/(L?min);乙v(Y)=2mol/(L?min);丙v(Z)=4.5mol/(L?min);丁v(X)=0.075mol/(L?s)。若其它条件相同,温度不同,则温度由高到低的顺序是(填序号) ???????????。
(3)若向达到(1)的平衡体系中充入氩气,则平衡向 ????????????(填"左"或"右"或"不")移动;若向
达到(1)的平衡体系中移走部分混合气体,则平衡向 ?????????(填" 左 " 或 " 右 " 或 " 不")移动。
(4)若在相同条件下向达到(1)所述的平衡体系中再充入0.5molX气体,则平衡后X的转化率⑷与⑴的
平衡中的X的转化率相比较??????????????。
A.无法确定
B.⑷一定大于⑴
C.⑷一定等于⑴
D.⑷一定小于⑴
(5)若保持温度和压强不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,达到平衡时仍
与(1)的平衡等效,则a、b、c应该满足的关系为 ???????????????????????。
(6)若保持温度和体积不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,达到平衡时仍
与(1)的平衡等效,且起始时维持化学反应向逆反应方向进行,则c的取值范围应该为 ?????????????。
本题答案:(共12分)(1)0.03mol/(L?min)???(2)
本题解析:
试题分析:(1)???2X(g) Y(g)+3Z(g)
Y(g)+3Z(g)
起始量(mol) 3????????? 0??? 0
转化量(mol) 2x???????? x??? 3x
平衡量(mol)3-2x?????? x??? 3x
平衡时测得容器内的压强为起始时的1.2倍
则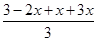 =1.2
=1.2
解得x=0.3mol
所以平衡时Y的物质的量浓度=0.3mol÷2L=0.15mol/L
因此Y的物质的量浓度变化表示的速率为0.15mol/L÷5min=0.03 mol/(L?min)
(2)在同一段时间内测得容器内的反应速率分别为:甲v(X)=3.5mol/(L?min);乙v(Y)=2mol/(L?min);丙v(Z)=4.5mol/(L?min);丁v(X)=0.075mol/(L?s),则根据反应速率之比是相应的化学计量数之比可知,如果都用X表示反应速率,则分别是3.5mol/(L?min)、4mol/(L?min)、3.0mol/(L?min)、4.5mol/(L?min)。温度越高反应速率越大,所以根据反应速率可知,温度由高到低的顺序是(填序号)丁>乙>甲>丙。
(3)若向达到(1)的平衡体系中充入氩气,由于其它物质的浓度不变,则平衡不移动;若向达到(1)的平衡体系中移走部分混合气体,导致生成物浓度降低,则平衡向右移动。
(4)由于该反应是体积增大的可逆反应,且反应物只有一种,所以平衡后再次通入X 气体,相当于增大压强,平衡向逆反应方向移动,所以若在相同条件下向达到(1)所述的平衡体系中再充入0.5molX气体,则平衡后X的转化率⑷与⑴的平衡中的X的转化率相比较⑷一定小于⑴,答案选D。
(5)若保持温度和压强不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,达到平衡时仍
与(1)的平衡等效,则根据方程式将生成物Y和Z恰好可以完全转化为X即可,所以a、b、c应该满足的关系为c=3b且a≥0。
(6)若保持温度和体积不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,达到平衡时仍
与(1)的平衡等效,则根据方程式将生成物Y和Z恰好可以完全转化为X,使X的物质的量等于3mol即可,所以c的最大值是4.5mol。由于平衡时c的物质的量是0.9mol,所以要满足起始时维持化学反应向逆反应方向进行,则c必须大于0.9mol,因此c的取值范围是0.9<c≤4.5。
本题所属考点:【反应速率与平衡的有关计算】
本题难易程度:【困难】
For one good deed a hundred ill deeds should be overlooked. 一善足以消百恶。