微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 铁是最常见的金属之一,铁可以形成多种氧化物、氢氧化物和盐类。铁与二氧化碳、水在某一密闭体系中反应情况如下表所示:
化学反应
| 平衡
常数
| 温度
|
973K
| 1173K
|
①Fe(s)+CO2(g) 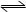 ?FeO(s)+CO(g) ?FeO(s)+CO(g)
| K1
| 1.47
| 2.15
|
②Fe(s)+H2O(g) 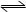 ?FeO(s)+H2(g) ?FeO(s)+H2(g)
| K2
| 2.38
| 1.67
|
③CO(g)+ H2O(g) 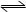 ?CO2(g)+ H2(g) ?CO2(g)+ H2(g)
| K3
| ?
| ?
完成下列填空:
(1)反应①是???????????(选填“吸热”,“放热”)反应。根据反应①与②可以推导出同温下K1、K2与K3之间的关系,则K3=?????????????????(用K1、K2表示)。
(2)973K时,若反应③在一个容积为2L的反应容器内2min时达到平衡,有3mol电子发生转移,则在2min内v(CO2)= ?????????????????????????。若压缩容器的容积为原来的一半,平衡将??????????????移动(选填“向左”,“向右”,“不”),CO2的浓度将???????????????????(选填“增大”,“减小”,“不变”)。使该反应的平衡转化率及平衡常数都增大的措施有????????????????????????????????????。
( 3)在FeCl3稀溶液中滴加KSCN溶液后呈红色,反应的离子方程式是????????????????;若在其中加入少量KCl固体,溶液的颜色________(选填“变深”,“变浅”,“不变”)。
(4)若先往FeCl3溶液中加入足量NaF溶液,再滴加KSCN溶液,则不呈红色,若再加入足够量FeCl3溶液.又会呈现红色。请对上述实验现象作出解释?????????????????。
填空题 铁是最常见的金属之一,铁可以形成多种氧化物、氢氧化物和盐类。铁与二氧化碳、水在某一密闭体系中反应情况如下表所示:
|