微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 反应N2O4(g)  ?2NO2(g) ΔH=+57 kJ・mol-1,在温度为T1、T2时,平衡体系中NO 2的体积分数随压强变化曲线如图所示。下列说法正确的是(???? )
?2NO2(g) ΔH=+57 kJ・mol-1,在温度为T1、T2时,平衡体系中NO 2的体积分数随压强变化曲线如图所示。下列说法正确的是(???? )
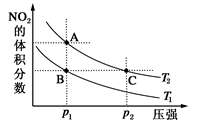
A.A、B两点的反应速率:A>B
B.B、C两点的反应平衡常数相同
C.由状态B到状态C,可以用加热的方法
D.A、C两点混合气体的平均相对分子质量:C>A
选择题 反应N2O4(g)  ?2NO2(g) ΔH=+57 kJ・mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是(???? )
?2NO2(g) ΔH=+57 kJ・mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是(???? )

A.A、B两点 91eXAm.org的反应速率:A>B
B.B、C两点的反应平衡常数相同
C.由状态B到状态C,可以用加热的方法
D.A、C两点混合气体的平均相对分子质量:C>A
本题答案:AD
本题解析:
试题分析:由已知反应方程式可知,反应的正反应是吸热反应,所以温度升高平衡正向移动,NO2的体积分数增大,根据图像,压强相同时,A、B两点的NO2的体积分数A点更大,则说明温度T2>T1,温度越大反应速率越大,所以A正确;B、C两点的温度不同,所以平衡常数不相等,B错误;状态B和状态C不仅温度不同,压强也不同,所以仅通过加热方法不能实现状态B到状态C的转变,C错误;C相对于A增大了压强,压强增大平衡逆向移动,则气体的物质的量减小,气体总质量不变,所以平均相对分子质量增大,D正确;故选AD。
本题所属考点:【反应速率与平衡的有关计算】
本题难易程度:【一般】
There are no faults in a thing we want badly. 我们非常想要的东西总是没有缺点的。