微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (14分)某科研小组设计出利用工业废酸(10%H2SO4)来堆浸某废弃的氧化铜锌矿制取活性ZnO的方案,实现废物综合利用,方案如下图所示。
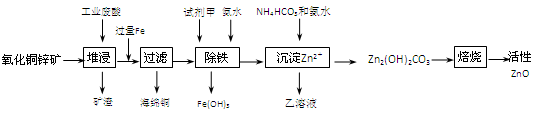
已知:298K时各离子开始沉淀及完全沉淀时的pH如下表所示。
离子
| 开始沉淀时的pH
| 完全沉淀时的pH
|
Fe2+
| 6.34
| 9.7
|
Fe3+
| 1.48
| 3.2
|
Zn2+
| 6.2
| 8.0
请回答下列问题:
(1)氧化铜锌矿中含有少量的CuS和ZnS,在H2SO4的作用下ZnS可以溶解而CuS不溶,这是由于相同温度下:Ksp(CuS)????????Ksp(ZnS)(选填“>”“<”或“=”)。
(2)你认为在除铁过程中选用下列物质中的????(填序号)作为试剂甲是比较合适的。
A.KMnO4????????? B.HNO3????????? C.H2O2????????????? D.Cl2
(3)除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在????????范围之间。
(4)请写出加甲物质后,加入氨水控制调节溶液的pH下生成Fe(OH)3反应的离子方程式??????????????????????????????????????????????????。
(5)298K时,残留在乙溶液中的c(Fe3+)在 __??????????mol/L以下。
[Fe(OH)3的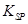 = 2.70×10-39] = 2.70×10-39]
(6)乙的溶液可直接用作氮肥,则乙的化学式是??????????。
(7)请写出“沉淀Zn2+”步骤中发生反应的化学方程式????????????????????????。
填空题 (14分)某科研小组设计出利用工业废酸(10%H2SO4)来堆浸某废弃的氧化铜锌矿制取活性ZnO的方案,实现废物综合利用,方案如下图所示。

已知:298K时各离子开始沉淀及完全沉淀时的pH如下表所示。
|