微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 利用如图所示的装置和其他必要的仪器用品,完成下列实验。

(1)证明氨气具有还原性。已知2NH3+3CuO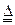 N2+3Cu+3H2O。
N2+3Cu+3H2O。
①碱石灰的作用是???????????????,稀硫酸的作用是?????????????????。
②浓氨水与固体NaOH接触,为什么会逸出大量氨气?????????????????????????????????
???????????????????????????????????????????????。
③证明NH3具有还原性的实验现象是???????????????????????????????????????。
(2)用吸收了足量尾气的溶液制取少量硫酸亚铁铵晶体。
已知:硫酸亚铁铵是淡蓝绿色晶体,在空气中性质比较稳定。硫酸亚铁铵在水中的溶解度小于硫酸铵、硫酸亚铁。制备硫酸亚铁铵的化学方程式为:(NH4)2SO4+FeSO4+6H2O==(NH4)2 Fe(SO4)2·6H2O。若溶液的pH>8.1,Fe外将转化为沉淀。
①吸收了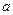 ?mol气体后,烧杯中的溶液能使酚酞变红。试依据“化学实验设计基本要求”设计制备硫酸亚铁铵溶液的方案,清简述实验方法。?????????????????????????????????
?mol气体后,烧杯中的溶液能使酚酞变红。试依据“化学实验设计基本要求”设计制备硫酸亚铁铵溶液的方案,清简述实验方法。?????????????????????????????????
??????????????????????????????????????????????????。
②为了从溶液中分离出硫酸亚铁铵晶体,还需要进行的实验操作是????????????????。
填空题 利用如图所示的装置和其他必要的仪器用品,完成下列实验。

(1)证明氨气具有还原性。已知2NH3+3CuO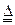 N2+3Cu+3H2O。
N2+3Cu+3H2O。
①碱石 灰的作用是???????????????,稀硫酸的作用是?????????????????。
②浓氨水与固体NaOH接触,为什么会逸出大量氨气?????????????????????????????????
???????????????????????????????????????????????。
③证明NH3具有还原性的实验现象是???????????????????????????????????????。
(2)用吸收了足量尾气的溶液制取少量硫酸亚铁铵晶体。
已知:硫酸亚铁铵是淡蓝绿色晶体,在空气中性质比较稳定。硫酸亚铁铵在水中的溶解度小于硫酸铵、硫酸亚铁。制备硫酸亚铁铵的化学方程式为:(NH4)2SO4+FeSO4+6H2O==(NH4)2 Fe(SO4)2·6H2O。若溶液的pH>8.1,Fe外将转化为沉淀。
①吸收了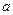 ?mol气体后,烧杯中的溶液能使酚酞变红。试依据“化学实验设计基本要求”设计制备硫酸亚铁铵溶液的方案,清简述实验方法。?????????????????????????????????
?mol气体后,烧杯中的溶液能使酚酞变红。试依据“化学实验设计基本要求”设计制备硫酸亚铁铵溶液的方案,清简述实验方法。?????????????????????????????????
??????????????????????????????????????????????????。
②为了从溶液中分离出硫酸亚铁铵晶体,还需要进行的实验操作是????????????????。
本题答案:①吸收水蒸气?吸收氨气?②NaOH吸收溶液中水分放热,使溶液
本题解析:①吸收水蒸气?吸收氨气?②NaOH吸收溶液中水分放热,使溶液温度升高,氢氧根离子浓度增大,都有利于氨气的逸出?③黑色粉末变为红色,有无色液滴产生? (2)①加入稀H2SO4调节溶液至酸性(答“调pH=8.1以下”给分).加入约0.5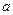 mol硫酸亚铁的浓溶液,搅拌.?②加热浓缩;冷却结晶;过滤。
mol硫酸亚铁的浓溶液,搅拌.?②加热浓缩;冷却结晶;过滤。
本题所属考点:【物质组成与性质实验方案的设计】
本题难易程度:【一般】
Fire is the test of gold, adversity of friendship. 烈火试真金,苦难试友情.