微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
实验题 (15分)氯酸钾是无机盐工业的重要产品之一,可通过反应:NaC1O3+KC1???KC1O3↓+NaC1制取。
(1)实验室制取氯酸钠可通过反应:3C12+6NaOH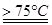 5NaC1+NaC1O3+3H2O,今在―5℃的NaOH溶液中通入适量C12(平衡常数K=1.09×1012),此时C12的氧化产物主要是???????????;将溶液加热,溶液中主要离子浓度随温度的变化如右图所示,图中A、B、C依次表示的离子是????????。
5NaC1+NaC1O3+3H2O,今在―5℃的NaOH溶液中通入适量C12(平衡常数K=1.09×1012),此时C12的氧化产物主要是???????????;将溶液加热,溶液中主要离子浓度随温度的变化如右图所示,图中A、B、C依次表示的离子是????????。

(2)工业上制取氯酸钠采用在热的石灰乳通入氯气,然
后结晶除去氯化钙后,再加入一种钠盐,合适的钠盐是
????????。
(3)北美、欧洲国家生产氯酸钠用二级精制盐水。采用
无隔膜电解法获得,生产过程中涉及的主要的化学反应式如下:
总反应式:NaC1+3H2O NaC1O3+3H2↑
NaC1O3+3H2↑
阳极:2C1――2e―???C12↑阴极:2H2O+2e―???H2↑+2OH―
液相反应:C12+H2O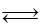 HC1O+H++C1―? HC1O
HC1O+H++C1―? HC1O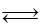 H++C1O―
H++C1O―
2HC1O+CO―???C1O3―+2C1―+2H+
精制食盐水时,要除去其中的Ca2+、Mg2+及SO42―并得到中性溶液,依次加入的化学试剂
是??????、????????、??????????;过滤,滤液中再加入适量的稀盐酸,得一级精制盐水再经离子交换处理或膜处理得到二级精制盐水。
②电解时,必须在食盐水中加入Na2Cr2O7,其目的是防止????????(填离子符号)电解过程中在阴极上放电。
(4)若NaC1O3与KC1的混合溶液中NaC1O3与KC1的质量分数分别为0.290和0.203(相关物质的溶解度曲线如右图)。从混合溶液中获得较多KC1O3晶体的实验操作依次
为?????(填操作名称)、干燥。
(5)样品中C1O3―的含量可用滴定法进行测定,实验步骤
如下:
步骤1:准确称取样品ag(约2.20g),经溶解、定容等步骤准确配制1000mL溶液。
步骤2:从上述容量瓶中取出10.00mL于锥形瓶中,准确加入25mL1000mol/L(NH4)2Fe(SO4)2。溶液(过量),加入75mL硫酸和磷酸配成的混酸,静置10min。
步骤3:再在锥形瓶中加入100mL蒸馏水及某种氧化还原反应指示剂,用0.200mol/LK2Cr2O7标准溶液滴定至终点。
步骤4:???????????。
步骤5:数据处理与计算。
①步骤2,静置10m in的目的是??????。
②步骤3中K2Cr2O2标准溶液应盛放在???????????中(填仪器名称)。
③为了确定样品中C1O3―的质量分数,步骤4的操作内容是?????????????。
实验题 (15分)氯酸钾是无机盐工业的重要产品之一,可通过反应:NaC1O3+KC1???KC1O3↓+NaC1制取。
(1)实验室制取氯酸钠可通过反应:3C12+6NaOH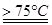 5NaC1+NaC1O3+3H2O,今在―5℃的NaOH溶液中通入适量C12(平衡常数K=1.09×1012),此时C12的氧化产物主要是???????????;将溶液加热,溶液中主要离子浓度随温度的变化如右图所示,图中A、B、C依次表示的离子是????????。
5NaC1+NaC1O3+3H2O,今在―5℃的NaOH溶液中通入适量C12(平衡常数K=1.09×1012),此时C12的氧化产物主要是???????????;将溶液加热,溶液中主要离子浓度随温度的变化如右图所示,图中A、B、C依次表示的离子是????????。

(2)工业上制取氯酸钠采用在热的石灰乳通入氯气,然
后结晶除去氯化钙后,再加入一种钠盐,合适的钠盐是
????????。
(3)北美、欧洲国家生产氯酸钠用二级精制盐水。采用
无隔膜电解法获得,生产过程中涉及的主要的化学反应式如下:
总反应式:NaC1+3H2O NaC1O3+3H2↑
NaC1O3+3H2↑
阳极:2C1――2e―???C12↑阴极:2H2O+2e―???H2↑+2OH―
液相反应:C12+H2O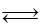 HC1O+H++C1―? HC1O
HC1O+H++C1―? HC1O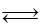 H++C1O―
H++C1O―
2HC1O+CO―???C1O3―+2C1―+2H+
精制食盐水时,要除去其中的Ca2+、Mg2+及SO42―并得到中性溶液,依次加入的化学试剂
是??????、????????、??????????;过滤,滤液中再加入适量的稀盐酸,得一级精制盐水再经离子交换处理或膜处理得到二级精制盐水。
②电解时,必须在食盐水中加入Na2Cr2O7,其目的是防止????????(填离子符号)电解过程中在阴极上放电。
(4)若NaC1O3与KC1的混合溶液中NaC1O3与KC1的质量分数分别为0.290和0.203(相关物质的溶解度曲线如右图)。从混合溶液中获得较多KC1O3晶体的实验操作依次
为?????(填操作名称)、干燥。
(5)样品中C1O3―的含量可用滴定法进行测定,实验步骤
如下:
步骤1:准确称取样品ag(约2.20g),经溶解、定容等步骤准确配制1000mL溶液。
步骤2:从上述容量瓶中取出10.00mL于锥形瓶中,准 确加入25mL1000mol/L(NH4)2Fe(SO4)2。溶液(过量),加入75mL硫酸和磷酸配成的混酸,静置10min。
步骤3:再在锥形瓶中加入100mL蒸馏水及某种氧化还原反应指示剂,用0.200mol/LK2Cr2O7标准溶液滴定至终点。
步骤4:???????????。
步骤5:数据处理与计算。
①步骤2,静置10min的目的是??????。
②步骤3中K2Cr2O2标准溶液应盛放在???????????中(填仪器名称)。
③为了确定样品中C1O3―的质量分数,步骤4的操作内容是?????????????。
本题答案:
在―5℃的NaOH溶液中通入适量C12时,主反应的方程式为:CL2 + 2NaOH ===== NaCL + NaCLO + H2O;此时CL2的氧化产物主要主要是NaCLO;将溶液加热,随温度的不断长高,主反应方程式为:3C12+6NaOH<img onload='if(this.width>600)makesmallpic(this,600,1800);' src=) 5NaC1+NaC1O3+3H2O,NaCLO不断减小,而NaCL不断增大,且NaCLO3不断增大。
5NaC1+NaC1O3+3H2O,NaCLO不断减小,而NaCL不断增大,且NaCLO3不断增大。
(2)热的石灰乳通入氯气,反应的方程式为:2CL2 + 2Ca(OH)2===== CaCL2 + Ca(CLO)2 + 2H2O;除去CaCL2后主要成分为Ca(CLO)2,要加入钠盐得到NaCLO3,则需遵循复分解反应所需条件,即所加钠盐可以是Na2SO4、Na2CO3;
(3)精制食盐水时,要除去其中的Ca2+、Mg2+及SO42―并得到中性溶液所需试剂为:Na2CO3除去Ca2+、NaOH除去Mg2+、BaCL2除去SO42―;但所加入的试剂遵循的原则是:Na2CO3一定放于BaCL2之后,HCL一定放在最后。
电解时,必须在食盐水中加入Na2Cr2O7,其目的是防止CLO-在电解过程中在阴极放电;
(4)根据各物质的溶解度曲线图分析可知:要从NaC1O3与KC1的混合溶液中得到KC1O3,采用的措施为:蒸发浓缩、冷却结晶、过滤、冰水洗涤;
(5)K2Cr2O2标准溶液具有强氧化性,必须放于酸式滴定管中,因为强氧化性物质会腐蚀碱式滴定管的橡胶管;静置10min的目的是使溶液中的CLO-完全被Fe2+还原为CL-;为了使得实验结果更加准备而减少误差,一般需重复操作步骤2和步骤3两至三次。
本题所属考点:【物质组成与性质实验方案的设计】
本题难易程度:【简单】
He that makes a thing too fine, breaks it. 做事过于苟求,反把事情弄坏。