微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
实验题 (16分)
黄铁矿在高温时和氧气反应生成氧化铁和二氧化硫(假设矿石中的杂质不参与化学反应)。某化学学习小组对黄铁矿样品进行如下实验探究:
【实验一】测定硫元素的含量
I.实验装置如下图所示(夹持和加热装置省略)。A中的试剂是双氧水,将m1g该黄铁矿样品放入硬质玻璃管D中。从A向B中逐滴滴加液体,使气体发生装置不断地缓缓产生气体,高温灼烧硬质玻璃管中的黄铁矿样品至反应完全。
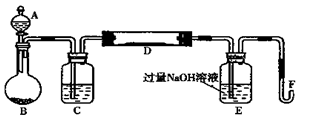
II.反应结束后,将E瓶中的溶液进行如下处理:
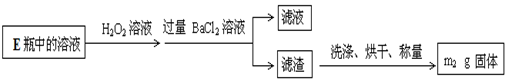
【实验二】测定铁元素的含量
III.测定铁元素含量的实验步骤如下:
① 用足量稀硫酸溶解硬质玻璃管D中的固体残渣;
② 加还原剂使溶液中的Fe3+完全转化为Fe2+后,过滤、洗涤;
③ 将滤液稀释至250 ml;
④ 每次取稀释液25.00 ml,用已知物质的量浓度为c mol/L的酸性KMnO4溶液滴定,三次滴定实验所需KMnO4溶液体积的平均值为V ml。
请回答下列问题:
(1)仪器B中发生反应的化学方程式是;仪器C中装入的试剂是。E瓶的作用是。
(2)II中加入H2O2发生反应的离子方程式。
(3)III的步骤③中,需要用到的仪器除烧杯、玻璃棒外,还必须要有;④中取稀释液25.00 ml需用的仪器是。
(4)来源:91考试网 91ExaM.org假设在整个实验过程中硫元素和铁元素没有损失,则该黄铁矿样品中硫元素的质量分数为。(用含m1和m2的代数式表示);该黄铁矿中铁元素的质量分数为。(用含m1、c、V的代数式表示)
实验题 (16分)
黄铁矿在高温时和氧气反应生成氧化铁和二氧化硫(假设矿石中的杂质不参与化学反应)。某化学学习小组对黄铁矿样品进行如下实验探究:
【实验一】测定硫元素的含量
I.实验装置如下图所示(夹持和加热装置省略)。A中的试剂是双氧水,将m1g该黄铁矿样品放入硬质玻璃管D中。从A向B中逐滴滴加液体,使气体发生装置不断地缓缓产生气体,高温灼烧硬质玻璃管中的黄铁矿样品至反应完全。

II.反应结束后,将E瓶中的溶液进行如下处理:

【实验二】测定铁元素的含量
III.测定铁元素含量的实验步骤如下:
① 用足量稀硫酸溶解硬质玻璃管D中的固体残渣;
② 加还原剂使溶液中的Fe3+完全转化为Fe2+后,过滤、洗涤;
③ 将滤液稀释至250 ml;
④ 每次取稀释液25.00 ml,用已知物质的量浓度为c mol/L的酸性KMnO4溶液滴定,三次滴定实验所需KMnO4溶液体积的平均值为V ml。
请回答下列问题:
(1)仪器B中发生反应的化学方程式是;仪器C中装入的试剂是。E瓶的作用是。
(2)II中加入H2O2发生反应的离子方程式。
(3)III的步骤③中,需要用到的仪器除烧杯、玻璃棒外,还必须要有;④中取稀释液25.00 ml需用的仪器是。
(4)假设在整个实验过程中硫元素和铁元素没有损失,则该黄铁矿样品中硫元素的质量分数为。(用含m1和m2的代数式表示);该黄铁矿中铁元素的质量分数为。(用含m1、c、V的代数式表示)
本题答案:
黄铁矿在高温时和氧气反应,所以A的作用是提供反应所需要的氧气,用过氧化氢制取氧气的方程式为<img onload='if(this.width>600)makesmallpic(this,600,1800);' src=) ;仪器C之后,气体进入了加热装置所以C装置的作用是干燥气体,所以C中放的是浓硫酸;由于反应中由二氧化硫产生所以E瓶的作用是吸收反应生成的二氧化硫,使其全部转化为亚硫酸根离子,有利于根据亚硫酸根离子的量计算样品中硫元素的质量。
;仪器C之后,气体进入了加热装置所以C装置的作用是干燥气体,所以C中放的是浓硫酸;由于反应中由二氧化硫产生所以E瓶的作用是吸收反应生成的二氧化硫,使其全部转化为亚硫酸根离子,有利于根据亚硫酸根离子的量计算样品中硫元素的质量。
(2)向亚硫酸钠溶液中加入H2O2发生反应的离子方程式为: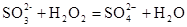
(3)步骤③是一个稀释溶液的题,并且要求稀释到一定的体积,所以需要的仪器除玻璃棒烧杯外还需要胶头滴管,250ML容量瓶。酸性KMnO4溶液具有强氧化性所以在吸取25.00 ml酸性KMnO4溶液时必须要用酸式滴定。
(4)硫元素质量分数:m2固体为硫酸钡固体,可以计算出其物质的量为 ,根据硫守恒可以算出硫元素质量为:
,根据硫守恒可以算出硫元素质量为: 所以样品中硫元素的质量分数为
所以样品中硫元素的质量分数为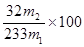 % ,铁元素的质量分数:酸性高锰酸钾与亚铁离子反应的方程式为
% ,铁元素的质量分数:酸性高锰酸钾与亚铁离子反应的方程式为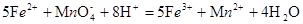 ?滴定消耗的高锰酸钾
?滴定消耗的高锰酸钾 ?,根据方程式可以计算出25ML稀释液中亚铁离子的物质的量为
?,根据方程式可以计算出25ML稀释液中亚铁离子的物质的量为 ,所以250 ML溶液中共有亚铁离子的物质的量为
,所以250 ML溶液中共有亚铁离子的物质的量为 ?,据此可得出原样品中铁元素的质量为
?,据此可得出原样品中铁元素的质量为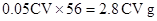 ?样品中铁元素的质量分数为
?样品中铁元素的质量分数为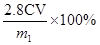
本题所属考点:【物质组成与性质实验方案的设计】
本题难易程度:【一般】
What God will no frost can kill. 天意难违。