微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
实验题 (共17分)硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步骤如下:
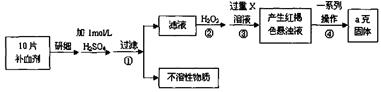
请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是先滴加KSCN溶液,再滴加????????????,该过程的现象为:?????????????????。
(2)步骤②加入过量H2O2的目的:???????????????????。
(3)步骤③中反应的离子方程式:????????????????????????????。
(4)步骤④中一系列处理的操作步骤:过滤、?????????、灼烧、?????????、称量。
(5)若实验无损耗,则每片补血剂含铁元素的质量?????????g。
(6)该小组有些同学认为用KMnO4溶液滴定也能进行铁元素含量的测定。
(5Fe2++MnO4—+8H+→5Fe3++Mn2++4H2O)
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻棒、烧杯、胶头滴管外,还需???????????????。
②上述实验中的KMnO4溶液需要酸化,用于酸化的酸是?????????。
a.稀硝酸?? b.稀硫酸??? c.稀盐酸??? d.浓硝酸
③滴定到终点时的现象描述为?????? ________________
实验题 (共17分)硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步骤如下:

请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是先滴加KSCN溶液,再滴加????????????,该过程的现象为:?????????????????。
(2)步骤②加入过量H2O2的目的:???????????????????。
(3)步骤③中反应的离子方程式:????????????????????????????。
(4)步骤④中一系列处理的操作步骤:过滤、?????????、灼烧、?????????、称量。
(5)若实验无损耗,则每片补血剂含铁元素的质量?????????g。
(6)该小组有些同学认为用KMnO4溶液滴定也能进行铁元素含量的测定。
(5Fe2++MnO4—+8H+→5Fe3++Mn2++4H2O)
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻棒、烧杯、胶头滴管外,还需???????????????。
②上述实验中的KMnO4溶液需要酸化,用于酸化的酸是?????????。
a.稀硝酸?? b.稀硫酸??? c.稀盐酸??? d.浓硝酸
③滴定到终点时的现象描述为?????? ________________
本题答案:(1)H2O2或氯水???滴加KSCN溶液不变色,再滴加H2
本题解析:
试题分析:本实验是通过将补血剂研碎,加入H2SO4溶解,通过过滤,将不溶物除去,而此时的溶液中,铁元素以Fe2+的形式存在,因为不稳定,所以加入强氧化剂H2O2将之氧化成Fe3+,接着加入过量的碱,生成Fe(OH)3的红褐色沉淀,经过过滤、洗涤、灼烧、冷却,将得到红棕色的Fe2O3粉末来测定铁元素的含量。
(1)证明滤液中有Fe2+,可以通过加入KSCN溶液,没颜色变化,再加入强氧化剂,像氯水、过氧化氢等将之氧化,此时溶液变成血红色来证明。
(2)因为Fe2+不稳定,所以常常通过加氧化剂把它氧化成稳定的Fe3+。
(3)Fe3+与碱反应,有两种形式,一种是和强碱反应,则Fe3++3OH-=Fe(OH)3↓,一种是和弱碱氨水反应,则Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+。
(5)FeSO4·7H2O中的铁元素最终是形成Fe2O3,
即2FeSO4·7H2O~Fe2O3
556?????? 160
X???????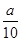
则来源:91考试网 www.91exAm.orgX=0.35a,即每片补血剂中含FeSO4·7H2O(0.35a) g,则每片含铁元素的质量为
(6)①因为要配置250ml的KMnO4溶液,故需要250ml的容量瓶,注意,常用的容量瓶有100ml、250ml、500ml和1000ml。
②加入的酸,尽量避免引入新的杂质,故选稀硫酸。
③Mn2+是无色,MnO4—是紫红色,判断到达终点的依据是滴入一滴KMnO4溶液,恰好变为紫红色,且半分钟内不褪色。2+和Fe3+相关性质的考核。
点评:本题考查了有关Fe2+和Fe3+的性质,要求学生掌握Fe2+和Fe3+的检验以及铁的重要化合物间的转化,除此,还要认识到一些实验室中的常识,如容量瓶的使用等。
本题所属考点:【物质组成与性质实验方案的设计】
本题难易程度:【简单】
No one is rich enough to do without a neighbour. 人略钜富,亦需邻居.