微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 工业上常用铁质容器盛装冷浓酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
[探究一]已去除表面氧化物的铁钉(碳素钢)放入浓硫酸中,加热,充分反应后收集到气体Y。某同学认为气体Y中除了SO2外还可能含有H2和CO2气体,为此设计了下列实验装置,探究Y中H2和CO2的存在(图中夹持仪器省略)。
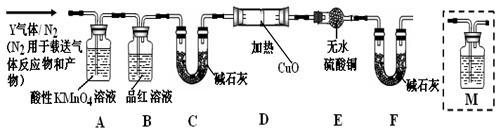
(1)装置B中试剂的作用是????????????????????????????????????。
(2)认为气体Y中还含有CO2的理由是???????????????????????????(用化学方程式表示)。
(3)为确认CO2的存在,需在装置中添加M于????????????(选填序号)。
a.. A之前????? b . A-B间?????? c . B-C间?????? d . C-D间
(4)如果气体Y中含有H2,预计实验现象应是???????????????????????????????????。
[探究二] SO2气体还原Fe3+、I2,使用的药品和装置如下图所示: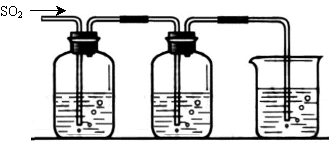
FeCl3溶液 含有淀粉的碘水 ? NaOH溶液
A B C
(5)装置C的作用是 ?????????????????????? ??。
(6)若要从A中所得溶液提取晶体,必须进行的实验操作步骤:蒸发浓缩、冷却结晶、 、洗涤、自然干燥,在这一系列操作中没有用到的仪器有 ? (填序号)。
A.蒸发皿
B.石棉网
C.漏斗
D.烧杯 E.玻璃棒 F. 坩埚
(7)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去
方案②:往第二份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红
方案③:往第三份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是 原因是 ?(8)能表明I-的还原性弱于SO2的现象是 。
填空题 工业上常用铁质容器盛装冷浓酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
[探究一]已去除表面氧化物的铁钉(碳素钢)放入浓硫酸中,加热,充分反应后收集到气体Y。某同学认为气体Y中除了SO2外还可能含有H2和CO2气体,为此设计了下列实验装置,探究Y中H2和CO2的存在(图中夹持仪器省略)。

(1)装置B中试剂的作用是????????????????????????????????????。
(2)认为气体Y中还含有CO2的理由是???????????????????????????(用化学方程式表示)。
(3)为确认CO2的存在,需在装置中添加 M于????????????(选填序号)。
a.. A之前????? b . A-B间?????? c . B-C间?????? d . C-D间
(4)如果气体Y中含有H2,预计实验现象应是???????????????????????????????????。
[探究二] SO2气体还原Fe3+、I2,使用的药品和装置如下图所示:
FeCl3溶液 含有淀粉的碘水 ? NaOH溶液
A B C
(5)装置C的作用是 ?????????????????????? ??。
(6)若要从A中所得溶液提取晶体,必须进行的实验操作步骤:蒸发浓缩、冷却结晶、 、洗涤、自然干燥,在这一系列操作中没有用到的仪器有 ? (填序号)。
A.蒸发皿
B.石棉网
C.漏斗
D.烧杯 E.玻璃棒 F. 坩埚
(7)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去
方案②:往第二份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红
方案③:往第三份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是 原因是 ?(8)能表明I-的还原性弱于SO2的现象是 。
本题答案:(1)检验SO2是否除尽??(2)C +2H2SO4(浓)<
本题解析:
试题分析:(1)A中酸性高锰酸钾溶液是除去SO2的,所以B中品红溶液的作用是可以检验A中是否完全除去SO2。
(2)由于碳素钢中还含有碳元素,也能被浓硫酸氧化生成CO2气体,即反应的化学方程式是C +2H2SO4(浓) CO2↑+2SO2↑+2H2O。
CO2↑+2SO2↑+2H2O。
(3)检验CO2一般用澄清的石灰水,所以要检验CO2的存在,需要在B-C间添加盛有澄清石灰水的M装置,答案选C。
(4)氢气还原氧化铜会生成水蒸气,能使白色的硫酸铜粉末变蓝色。
(5)SO2是大气污染物,所以氢氧化钠溶液的作用是吸收SO2尾气,防止污染空气。
(6)所得得晶体应该通过过滤得到,又因为液体得蒸发浓缩需要蒸发皿,不需要坩埚,且蒸发皿可以直接加热,所以不需要得仪器是BF。
(7)因为A的溶液中含有SO2,SO2也能使KMnO4溶液褪色,所以方案①不合理。
(8)B中蓝色溶液褪色,说明B中单质点被还原,SO2被氧化,因此能说明I-的还原性弱于SO2的。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,难度较大。试题在注重对学生基础知识巩固与训练的同时,侧重对学生能力的培养与解题方法的指导与训练,有利于培养学生的逻辑推理能力和规范的实验设计、操作能力。该类试题综合性强,理论和实践的联系紧密,有的还提供一些新的信息,这就要求学生必须认真、细致的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能得出正确的结论。
本题所属考点:【物质组成与性质实验方案的设计】
本题难易程度:【简单】
If each would sweep before his own door,we should have a clean city. 若家家动手扫清门前,整个城市就清洁了.