��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
ʵ���� ������ͼ��ʾװ�ã�β�����������ԣ�����ȡһ����̼�������Բⶨijͭ����Ʒ������CuO��ĩ���н���ͭ�ĺ���

��1���Ʊ�һ����̼�Ļ�ѧ����ʽ����??????????????????����
��2�������У��۲쵽��Ӧ���з�������������???????????????����β������Ҫ�ɷ����� ????????����
��3����Ӧ��ɺ���ȷ�IJ���˳��Ϊ��???????????��������ĸ��
a���ر�©������? b��Ϩ��ƾ�1?? c��Ϩ��ƾ���2
��4���������г�ȡͭ����Ʒ5.0g����ַ�Ӧ��Ӧ����ʣ����������Ϊ4.8g����ԭ��Ʒ�е���ͭ����������Ϊ��?????????����
��5����Ũ���ᡢŨ���ᡢ����ˮ��˫��ˮ��ѡ�ú��ʵ��Լ������һ���ⶨ��Ʒ�н���ͭ���������ķ�����
����Ʒ�������Ҫ�����ǣ����������������̵�ϸ�ڣ���??????????????????????????????????����
��д���йط�Ӧ�Ļ�ѧ����ʽ��?????????????????����
ʵ���� ������ͼ��ʾװ�ã�β�����������ԣ�����ȡһ����̼�������Բⶨijͭ����Ʒ������CuO��ĩ���н���ͭ�ĺ���

��1���Ʊ�һ����̼�Ļ�ѧ����ʽ����??????????????????����
��2�������У��۲쵽��Ӧ���з�������������???????????????����β������Ҫ�ɷ�����????????����
��3����Ӧ��ɺ���ȷ�IJ���˳��Ϊ��???????????��������ĸ��
a���ر�©������? b��Ϩ��ƾ�1?? c��Ϩ��ƾ���2
��4���������г�ȡͭ����Ʒ5.0g����ַ�Ӧ��Ӧ����ʣ����������Ϊ4.8g����ԭ��Ʒ�е���ͭ����������Ϊ��?????????����
��5����Ũ���ᡢŨ���ᡢ����ˮ��˫��ˮ��ѡ�ú��ʵ��Լ������һ���ⶨ��Ʒ�н���ͭ���������ķ�����
����Ʒ�������Ҫ�����ǣ����������������̵�ϸ�ڣ���??????????????????????????????????����
��д���йط�Ӧ�Ļ�ѧ����ʽ��?????????????????����
����𰸣���1��HCOOHmakesmallpic(this,600,1800);' src=) Cu+CO2����Ӧ���з����������Ǻ�ɫ��ĩ ��죻β������Ҫ�ɷ���CO��CO2��
Cu+CO2����Ӧ���з����������Ǻ�ɫ��ĩ ��죻β������Ҫ�ɷ���CO��CO2��
��3��ʵ�鲽�裺��ͨ��COһ������ȴ���Ӧ���ڵ�ҩƷ��ȫ��ֹͣ���ȣ�Ȼ�����ͨ��CO����������ȴΪֹ��
��4���������г�ȡͭ����Ʒ5.0g����ַ�Ӧ��Ӧ����ʣ����������Ϊ4.8g��ʣ�����ȫ��Ϊͭ�����ò����������ԭ��Ʒ������ͭ����������������ͭ������������
��5����Ҫ�ⶨͭ����������������Ũ����ϡ�ͣ�ͭ��ϡ�����Ӧ������ͭ��ϡ���ᷴӦ���������ͭ��������������Ʒ�������Ҫ�����ǽ�Ũ����������ˮϡ�ͣ�����Ʒ��ϡ�����ַ�Ӧ���ˣ��������ʣ�����ͭ���������ɣ��ڷ�Ӧ�Ļ�ѧ����ʽΪCuO+H2SO4=CuSO4+H2O��
�⣺��1��������Ũ���ᡢ���ȵ������·ֽ�����CO��H2O����Ӧ����ʽΪHCOOH CO��+H2O��
CO��+H2O��
�ʴ�Ϊ��HCOOH CO��+H2O��
CO��+H2O��
��2��ʵ���У���Ӧ���з�����ӦCuO+CO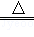 Cu+CO2����Ӧ���з����������Ǻ�ɫ��ĩ��죻β������Ҫ�ɷ���CO��CO2��
Cu+CO2����Ӧ���з����������Ǻ�ɫ��ĩ��죻β������Ҫ�ɷ���CO��CO2��
�ʴ�Ϊ����Ʒ�ɺ�ɫ���ɫ��CO��CO2��
��3����Ӧ�����˳���ȳ��ƾ���2����ʱ���װ��������ȡCO��Ȼ���ٹرշ�Һ©���Ŀ��أ����ټ��뷴Ӧ�Լ�����ƾ���1ֹͣ��Ӧ������������ֹ������O2�����ұ�װ��ͭ�ֱ�����Ϊ����ͭ�ˣ���ȷ�IJ���˳��Ϊ��Ϩ��ƾ���2���ر�©�����أ����Ϩ��ƾ�1����cab��
�ʴ�Ϊ��cab��
��4���������г�ȡͭ����Ʒ5.0g����ַ�Ӧ��Ӧ����ʣ����������Ϊ4.8g��ʣ�����ȫ��Ϊͭ������Ʒ��CuO������Ϊm����
CuO+CO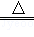 Cu+CO2�������������١�m
Cu+CO2�������������١�m
80???????????????? 16
m???????????????? 5g��4.8g=0.2g
��m=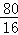 ��0.2g=1g��
��0.2g=1g��
����ԭ��Ʒ�н���ͭ����������Ϊ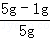 ��100%=80%��
��100%=80%��
�ʴ�Ϊ��80%��
��5����Ҫ�ⶨͭ����������������Ũ����ϡ�ͣ�ͭ��ϡ�����Ӧ������ͭ��ϡ���ᷴӦ���������ͭ��������������Ʒ�������Ҫ�����ǽ�Ũ����������ˮϡ�ͣ�����Ʒ��ϡ�����ַ�Ӧ���ˣ��������ʣ�����ͭ���������ɣ�
�ʴ�Ϊ����Ũ����������ˮϡ�ͣ�����Ʒ��ϡ�����ַ�Ӧ���ˣ��������ʣ�����ͭ���������ɣ�
�ڷ�Ӧ�Ļ�ѧ����ʽΪCuO+H2SO4=CuSO4+H2O��
�ʴ�Ϊ��CuO+H2SO4=CuSO4+H2O��
���������⿼��ѧ����ʵ��ԭ����ʵ����������⡢ʵ�鷽����ơ�Ԫ�ػ��������ʡ���ѧ����ȣ��Ѷ��еȣ����ʵ��ԭ���ǽ���Ĺؼ�����Ҫѧ���߱���ʵ�Ļ���֪ʶ���ۺ�����֪ʶ�������⡢��������������
�����������㣺���������������ʵ�鷽������ơ�
�������׳̶ȣ���һ�㡿
A man who knows two languages is worth two men. �����������Ե��˵ֵ���������.