微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
实验题 氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟工业原理制备氨基甲酸铵,反应的化学方程式如下:2 NH3(g)+CO2(g)  ?NH2COONH4(s)?? ΔH<0
?NH2COONH4(s)?? ΔH<0
(1)实验室制备NH3的化学方程式是:??????????????????????????。
(2)制备氨基甲酸铵的装置如下图所示,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。当悬浮物较多时,停止制备。
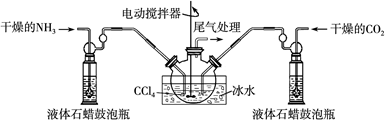
注:四氯化碳与液体石蜡均为惰性介质。
①发生器用冰水冷却的原因是??????????。液体石蜡鼓泡瓶的作用是?????????????。
②从反应后的混合物中分离出产品的实验方法是???????(填写操作名称)。为了得到干燥产品,应采取的方法是?????(填写选项序号)。
a. 常压加热烘干??????? b. 高压加热烘干?????? c. 真空40 ℃以下烘干
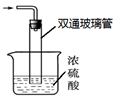
③尾气处理装置如右图所示。双通玻璃管的作用:???????????;?
浓硫酸的作用:????? ????????????? ?????????。
(3)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.7825 g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.000 g。则样品中氨基甲酸铵的物质的量分数为????????????。
实验题 氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟工业原理制备氨基甲酸铵,反应的化学方程式如下:2 NH3(g)+CO2(g)  ?NH2COONH4(s)?? ΔH<0
?NH2COONH4(s)?? ΔH<0

(1)实验室制备NH3的化学方程式是:??????????????????????????。
(2)制备氨基甲酸铵的装置如下图所示,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。当悬浮物较多时,停止制备。

注:四氯化碳与液体石蜡均为惰性介质。
①发生器用冰水冷却的原因是??????????。液体石蜡鼓泡瓶的作用是?????????????。
②从反应后的混合物中分离出产品的实验方法是???????(填写操作名称)。为了得到干燥产品,应采取的方法是?????(填写选项序号)。
a. 常压加热烘干??????? b. 高压加热烘干?????? c. 真空40 ℃以下烘干
③尾气处理装置如右图所示。双通玻璃管的作用:???????????;?
浓硫酸的作用:????? ????????????? ?????????。
(3)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.7825 g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.000 g。则样品中氨基甲酸铵的物质的量分数为????????????。
本题答案:(1)2NH4Cl + Ca(OH)2△2NH
本题解析:
试题分析:(1)实验室制备NH3的化学方程式是2NH4Cl + Ca(OH)2 2NH3 ↑+ CaCl2 + 2H2O。
2NH3 ↑+ CaCl2 + 2H2O。
(2)①因为反应放热,降低温度,提高反应物转化率,同时,防止因反应放热造成产物分解;通过观察气泡,调节NH3与CO2通入比例②反应后的固体和液体的混合物,分离出产品的实验方法是过滤。因为氨基甲酸铵热稳定性差,为了得到干燥产品,应采取的方法是真空40 ℃以下烘干;③图中尾气处理装置使用了截面积较大的玻璃管,可防止倒吸;浓硫酸可以吸收多余氨气,防止空气中水蒸气进入反应器使氨基甲酸铵水解。
(3)由NH2COONH4――CaCO3可知0.7825 g NH2COONH4是0.0133mol,1.000 g CaCO3是0.01mol,样品中氨基甲酸铵的物质的量分数为75%。来源:91考试网 91ExaM.org
本题所属考点:【物质组成与性质实验方案的设计】
本题难易程度:【一般】
Capacity without education is pitiful; education without capacity is throw away. 有才干缺教育令人可惜; 有教育缺才干被人抛弃.