微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 常温下各取n g金属钠、铝、铁,加入V mL 1 mol/L的稀H2SO4中,要使铝铁反应后放出等量的氢气,且比钠反应生成的氢气少,则V比n的关系是????????????????????????????
A.V≤1000 n/46
B.V≤n/23
C.V<n/46
D.V≥1000 n/18
参考答案:A
本题解析:

要使Al Fe和H2SO4反应放出等量氢气,唯有Al,Fe都过量或完全
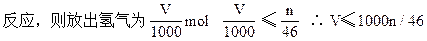
本题难度:一般
2、选择题 将等体积的AlCl3溶液和NaOH溶液混合后,沉淀物中铝元素的物质的量与溶液中铝元素的物质的量相等,则原AlCl3溶液与NaOH溶液的物质的量浓度之比可能是(? )
A.1:3
B.2:5
C.1:5
D.2:7
参考答案:D
本题解析:
试题分析:由于氢氧化铝是两性氢氧化物,能溶于氢氧化钠溶液中,所以溶液中的铝元素,可以是铝离子,也可以是AlO2-,因此根据反应的方程式Al3++3OH-=Al(OH)3↓、Al(OH)3+OH-=AlO2-+2H2O可知,如果氯化铝过量,则原AlCl3溶液与NaOH溶液的物质的量浓度之比2:3;如果氢氧化钠过量,生成偏铝酸钠,则原AlCl3溶液与NaOH溶液的物质的量浓度之比 本题难度:一般
本题难度:一般
3、填空题 把河沙跟镁粉按一定质量比例混合均匀(15∶24),装入试管中加热,大约1 min发生剧烈反应,待生成的混合物冷却后放入盛有稀硫酸的烧杯中,即产生气泡,并伴有爆鸣声,产生一种气态氢化物。
(1)写出河沙跟镁粉在加热条件下反应的方程式,并标明是放热还是吸热:____________
_______________________________________________________________________________。
(2)写出生成的混合物放入稀硫酸中发生反应的方程式:____________________________。
(3)写出产生“爆鸣声”的化学方程式:__________________________________________。
参考答案:(1)SiO2+4Mg 本题解析:1 min后发生剧烈反应,说明该反应是放热反应。河沙的成分主要是SiO2,SiO2与镁反应后的混合物与稀硫酸反应产生的气态氢化物只能是SiH4。SiH4很活泼,在空气中能自燃,产生“爆鸣声”。
本题解析:1 min后发生剧烈反应,说明该反应是放热反应。河沙的成分主要是SiO2,SiO2与镁反应后的混合物与稀硫酸反应产生的气态氢化物只能是SiH4。SiH4很活泼,在空气中能自燃,产生“爆鸣声”。
本题难度:简单
4、选择题 把a g 铝铁合金粉末溶于足量盐酸中,再加入过量氢氧化钠溶液。过滤出沉淀,经洗涤、干燥、灼烧,得到红棕色粉末的质量仍 为a g,则此合金中铝的质量分数为(?)
为a g,则此合金中铝的质量分数为(?)
A.70%
B.30%
C.52.4%
D.22.2%
参考答案:B
本题解析:略
本题难度:简单
5、填空题 (1)若向NaHSO4溶液中逐滴加入Ba(OH)2溶液,使原溶液中的SO42-恰好完全沉淀,试写出该反应的化学方程式_________________________
(2)明矾是一种无色晶体,可溶于水并形成Al(OH)3胶体来净水。已知明矾水溶液的主要成分是
KAl(SO4)2,现向明矾溶液中逐滴加入Ba(OH)2溶液,当Al3+恰好全部沉淀时,试写出该反应的化学方程式
_________________________。
参考答案:(1)NaHSO4+Ba(OH)2==BaSO4↓+H2O+
本题解析:
本题难度:一般