微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 把a L硫酸铵和硝酸铵混合液分成两等份,一份需用b mol烧碱刚好把氨全部赶出,另一份与BaCl2溶液反应恰好消耗c mol BaCl2。原溶液中NO3-的物质的量浓度是( )
A. mol・L-1
mol・L-1
B. mol・L-1
mol・L-1
C. mol・L-1
mol・L-1
D. mol・L-1
mol・L-1
参考答案:D
本题解析:
试题分析:由题意得,原溶液中NH4+的物质的量为2bmol,SO42-的物质的量为2cmol,根据电荷守恒NO3-的物质的量为(2b-4c)mol,所以原溶液中NO3-的物质的量浓度是(2b-4c)mol/aL,答案选D。
考点:考查电荷守恒规律的应用
本题难度:一般
2、选择题 设NA表示阿伏加德罗常数的值,下列有关说法中正确的是(???)
A.标准状况下,NA个SO3分子所占的体积约为22.4 L
B.18g重水所含的电子数为10 NA
C.常温下,pH=11的氨水中OH―数等于10―3NA
D.1lg丙烷中共用电子对数为2.5 NA
参考答案:D
本题解析:A不正确,标准状况下,三氧化硫不是气体,不能用于气体摩尔体积。18g重水不是1mol,B不正确。C不正确,因为无法确定溶液的体积。丙烷分子中含有10对电子对,所以11g丙烷中共用电子对是 ,D正确,答案选D。
,D正确,答案选D。
本题难度:一般
3、选择题 只给出下列甲和乙中对应的量,不能求出物质的量的是( )
A.甲:物质的粒子数;乙:阿伏加德罗常数
B.甲:标准状况下的气体摩尔体积;乙:标准状况下的气体体积
C.甲:固体的体积;乙:固体的密度
D.甲:物质的质量;乙:物质的摩尔质量
参考答案:C
本题解析:
本题难度:简单
4、选择题 某硫酸铝溶液中,含 Al3+ ag,则溶液中SO42-的物质的量为[???? ]
A.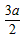 mol
mol
B.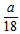 mol
mol
C.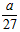 mol
mol
D.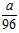 mol
mol
参考答案:B
本题解析:
本题难度:简单
5、填空题 Ⅰ.实验室配制1mol/L Na2CO3溶液250ml。
(1)需要固体Na2CO3?????????g;(2)该溶液中的阳离子数目为?????????????个;
(3)需要物质的量浓度为5mol/L 的Na2CO3溶液???????????ml;
(4)将该溶液与足量稀硫酸反应,产生的气体在标准状况下的体积为??????????L。
(5)配制该溶液的操作顺序是(用字母表示,不重复使用) ??????????????????????。
A.称量
B.洗涤
C.定容
D.溶解 E.摇匀 F.转移
Ⅱ.现有四种可溶性盐,其阳离子分别是K+、Ba2+、Fe3+、Ag+ 中的某一种,阴离子分别是Cl-、SO42-、CO32-、NO3- 中的某一种。小华同学说,不用做实验就可以确定这四种盐,那么他确定的四种盐的化学式分别为:????????????????????????????????????。
参考答案:(1)26.5?(2)0.5NA或3.01×1023????
本题解析:
试题分析:
Ⅰ.(1)m(Na2CO3)=0.25×1×106g=26.5g;(2)n(Na2CO3)= 0.25×1=0.25mol
n(Na+)="0.5" mol,所以阳离子数目为0.5NA.(3)根据稀释前后溶质的物质的量不变,有1mol/L ×250ml="5" mol/L×V,V=50ml.(4)n(Na2CO3)= 0.25×1=0.25mol,所以,n(CO2)= 0.25mol,V="5.6L." (5)配制溶液的顺序是A.称量D.溶解F.转移 B.洗涤 C.定容 E
本题难度:一般