微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 粗盐中含有不溶于水的泥沙,还有其他的可溶于水的杂质Na2SO4、MgCl2、CaCl2,如何设计一个合理的实验方案提纯粗盐。其正确的操作顺序是( ????)
①过滤 ②加过量的NaOH;③加适量盐酸;④加过量Na2CO3溶液 ⑤加过量BaCl2溶液。
A.①④②⑤③
B.④①②⑤③
C.④②⑤①③
D.⑤②④①③
参考答案:D
本题解析:略
本题难度:简单
2、选择题 下列分离方法不正确的是( )
A.用过滤的方法除去食盐水中的泥沙
B.用蒸馏的方法将自来水制成蒸馏水
C.用四氯化碳萃取碘水中的碘
D.用分液漏斗分离汽油和植物油
参考答案:A、食盐水中的泥沙是难溶物质,分离不溶物和溶液可用过滤的方法
本题解析:
本题难度:一般
3、实验题 某校化学兴趣小组的同学设计以下实验来定性检验茶叶中含有钙、铁、铝三种金属元素。【已知完全沉淀的pH:Ca(OH)2:pH ≥ 13;Al(OH)3:pH ≥ 5.5;Fe(OH)3:pH ≥ 4.1】
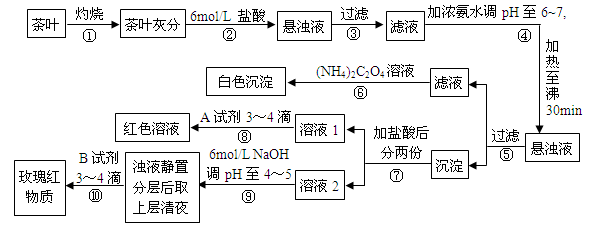
下列说法不正确的是
A.步骤②加入6mol/L盐酸的主要目的是为了将茶叶灰分中的钙、铁、铝难溶性化合物转化为可溶性氯化物
B.步骤⑤所得滤液中溶质的主要成分为:CaCl2、NH3・H2O
C.步骤⑥可以检出钙元素存在,离子反应方程式为Ca2++C2O42- = CaC2O4↓
D.步骤⑧中A试剂为KSCN溶液,离子反应方程式为Fe3++3SCN- Fe(SCN)3
Fe(SCN)3
参考答案:B
本题解析:
试题分析:根据题意知,茶叶灼烧得到灰分经步骤②:加入6mol/L盐酸,将茶叶灰分中的钙、铁、铝难溶性化合物转化为可溶性氯化物;经步骤④:在pH为6-7时加热30 min,可使Al3+、Fe3+转化成Al(OH)3和Fe(OH)3沉淀,经⑤过滤后所得滤液中含CaCl2、NH4Cl,步骤⑥中发生反应是草酸铵和钙离子形成草酸钙沉淀的反应;⑧是加入硫氰酸钾溶液出现血红色证明含有铁离子;步骤⑨是调节溶液PH值4-5,结合离子沉淀PH范围分析作用是把铁离子完全沉淀;步骤⑩是检验铝元素存在的操作。A、步骤②加入6mol/L盐酸的主要目的是为了将茶叶灰分中的钙、铁、铝难溶性化合物转化为可溶性氯化物,正确;B、步骤⑤所得滤液中溶质的主要成分为:CaCl2、NH4Cl,错误;C、步骤⑥可以检出钙元素存在,离子反应方程式为Ca2++C2O42- = CaC2O4↓,正确;D、步骤⑧中A试剂为KSCN溶液,离子反应方程式为Fe3++3SCN- Fe(SCN)3,正确。
Fe(SCN)3,正确。
本题难度:一般
4、选择题 将物质的量均为a mol的钠和铝一同放在m g足量的水中,所得溶液密度为dg/mL,则此溶液的物质的量浓度(mol/L)为
A.1000da/(50a+m)
B.da/(46a+m)
C.1000da/(48a+m)
D.1000da/(46a+m)
参考答案:D
本题解析:
本题难度:困难
5、填空题 选择下列实验方法分离物质,将分离方法的序号填在横线上。
A萃取分液法;B加热分解;C结晶法;D分液法;E蒸馏法;F过滤法
(1)从硝酸钾和氯化钠的混合溶液中获得硝酸钾;???????
(2)分离水和汽油的混合物;???????
(3)分离饱和食盐水与泥沙的混合物;???????
(4)分离相溶的CCl4(沸点为76.75℃)和甲苯(110.6℃)的混合物;???????
参考答案:(1)C??????(2)D????(3) F?????(4
本题解析:
试题分析:(1)从硝酸钾和氯化钠的混合溶液中获得硝酸钾;硝酸钾的溶解度受温度影响大,氯化钠的溶解度受温度影响小,故选择结晶法进行分离。(2)分离水和煤油的混合物;互不相溶且密度有差异,用分液法。(3)饱和食盐水(溶液)和沙子(难溶物)分离用过滤法。(4)分离相溶的CCl4(沸点为76.75℃)和甲苯(110.6℃)的混合物;两者相溶沸点有差异可选择蒸馏法。
本题难度:一般