微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列实验能达到目的的是
序号
| 实验目的
| 实验操作
|
A
| 证明Ksp(AgI)<Ksp(AgCl)
| 在AgNO3溶液中滴加少量NaCl溶液,产生白色沉淀,继续滴加少量KI溶液又产生黄色沉淀
|
B
| 阿司匹林的提纯,即除去混有的水杨酸聚合物等杂质
| 将阿司匹林粗品溶解在适量饱和碳酸氢钠溶液中,抽滤后在滤液中加入盐酸,再抽滤并洗涤
|
C
| 检验火柴头中含氯元素
| 往浸过火柴头的溶液中加AgNO3溶液和稀硝酸
|
D
| 加快锌与稀硫酸反应制取H2的速率
| 在稀硫酸中滴加少量Cu(NO3)2溶液
参考答案:B
本题解析:A不能,与氯化钠是不足的,硝酸银过量。氯酸钾中的氯原子不能电离出氯离子,得不到沉淀,C不正确。再酸性溶液中硝酸盐具有氧化性,和锌反应得不到氢气,D不正确。答案选B。
本题难度:一般
2、填空题 中学化学实验中,在过滤器上洗涤沉淀的操作方法是____________。
参考答案:向过滤器中加入蒸馏水至浸没沉淀,待水自然流下后,重复操作几次
本题解析:
本题难度:一般
3、选择题 现有一瓶物质甲和乙的混合物,已知甲和乙的某些性质如下:
物质
| 化学式
| 熔点( ℃)
| 沸点( ℃)
| 密度(g・cm-3)
| 水中溶解性
| 甲
| C3H6O2
| -98
| 57.5
| 0.93
| 可溶
| 乙
| C4H8O2
| -84
| 77
| 0.90
| 可溶
据此,将甲和乙互相分离的最佳方法是(???)
A.萃取法
B.生化法
C.分馏法
D.分液法
参考答案:C
本题解析:本题要求根据试题给定的甲乙两物质的性质,综合分析后选出分离方案。升华法显然不行;因为甲乙两物质均溶于水,所以能用分液、萃取也不可行;只能根据沸点的差异采取分馏法比较合适。
本题难度:简单
4、实验题 下列有关实验装置进行的相应实验,能达到实验目的的是
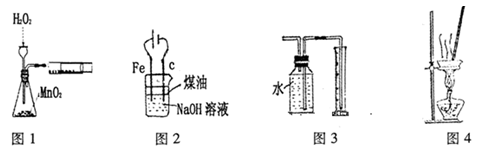
A.图l装置可用于定量测定H2O2的分解速率
B.图2装置制备Fe(OH)2并能较长时间观察其颜色
C.图3装置测量Cu与浓硝酸反应产生气体的体积
D.图4装置可用于蒸干NH4Cl饱和溶液制备NH4Cl晶体
参考答案:B
本题解析:
试题分析:A、图l装置可用于定量测定H2O2的分解速率,应用分液漏斗滴加双氧水,缺少秒表,错误;B、图2装置制备Fe(OH)2,阳极铁提供亚铁离子,氢氧化钠溶液提供氢氧根,煤油隔绝空气,能较长时间观察其颜色,正确;C、Cu与浓硝酸反应产生的二氧化氮气体易溶于水,不能用排水法量其体积,错误;D、NH4Cl水解生成一水合氨和盐酸,升高温度促进其水解,氨水和盐酸易挥发,蒸干NH4Cl饱和溶液得不到NH4Cl晶体,错误。
本题难度:一般
5、实验题 (本题共12分)海水中有丰富的卤素资源,含量最高的食盐(NaCl)不但是人类生活不可缺少的物质,而且是重要的化工原料。
(1).实验室里常用NaCl制取HCl。请在下图中选择合适的仪器用于发生HCl气体:
(填写仪器编号)。
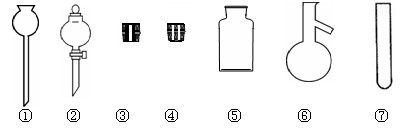
(2).在实验室里使用与制取HCl相同的实验装置和条件,将浓硫酸滴入NaBr(s),可以观察到的现象是???????????????????????????????????????????????????????????????????。
(3).产生上述现象的原因是??????????????????? ??????????????????? 。
(4).收集HCl(g)和HBr(g)的实验时不可缺少的实验操作是: 。
(5).除水之外,限用 HCl(g)、HBr(g)和HI(g),还需要 (填写试剂的化学式),就能设计实验比较氯、溴、碘的化学活泼性。
(6).工业上可用食盐作为一种主要原料,经不同的方法生产纯碱。联合制碱法(侯氏制碱法)与氨碱法(索氏制碱法)相比,其优点是: 、 和避免产生大量含CaCl2的废液。
参考答案:(1).② ③ ⑥?????????????????????
本题解析:(1),实验室制取氯化氢的原料是浓硫酸和固体氯化钠,所以答案是②③⑥。
(2).由于浓硫酸还具有氧化性,能氧化溴化氢生成单质溴,所以现象是先有白雾(或无色气体)产生,很快有红棕色气体生成。
(3).略
(4).由于二者都是极易溶于水的,所以必须用适当的方式吸收尾气,以防止倒吸。
(5).要比较其非金属性强弱,需要根据单质见的置换反应,所以应先制取氯气,为了检验生成物,可以利用卤素单质都易溶在有机溶剂中,进行萃取即可。所以答案是MnO2或其他合理的氧化剂、CCl4或其他合理的萃取剂。
(6).其优点是提高了食盐的利用率(或充分利用食盐中的钠和氯)、可节省石灰窑和蒸氨塔等设备(或减少CaCO3制 CO2这一工序,降低了能耗与污染)。
本题难度:一般
|
|