��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
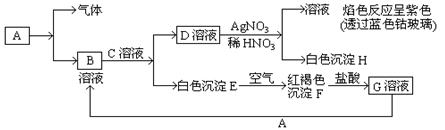
1������� ��10�֣���֪������������A�����������ת��
�Իش�
(1)д��B�Ļ�ѧʽ?????????????????��D�Ļ�ѧʽ??????????????????????��
(2)д����Eת���F�Ļ�ѧ����ʽ??????????????????????????????????????????????��
(3)д������G��Һ�еĽ��������ӵ��Լ��ǣ�д��ѧʽ��???????????????����G��Һ����A���й����ӷ�Ӧ����ʽ??????????????????????????????????????????????????��
�ο��𰸣�(1).FeCl2?????? KCl��3����KSCN
�����������ɫ��ӦΪ��ɫ��֤������Һ������ΪK����HΪ��ɫ����ΪAgCl�����Ƴ�DΪKCl��Һ����ɫ����E�����ɫ����F�Ƴ�EΪFe(OH)2��FΪFe(OH)3,��D��E�Ƴ�CΪKOH��Һ��BΪFeCl2��Һ��AΪ������������AΪFe��Fe��HCl=FeCl2��H2
(1)B�Ļ�ѧʽΪFeCl2,D�Ļ�ѧʽΪKCl
(2)4Fe(OH)2��O2��2H2O=4Fe(OH)3
(3)����Fe3�����Լ���KSCN��Һ???? 2Fe3����Fe=3Fe2��
�����Ѷȣ���
2��ѡ���� ijͬѧ������з�����A�ε�ˮ��Һ���м�����
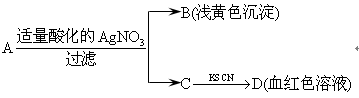
�ɴ˵ó��Ľ����У�����ȷ����?��???��
A����ҺC����Fe3��
B��Aһ��ΪFeBr2
C��D��Һ�д���Fe(SCN)3
D��BΪAgBr
�ο��𰸣�B
���������
�𰸣�B
�ữ��AgNO3�У�H����NO3�D���HNO3�ܽ�Fe2�� ��������ȷ��Fe3�� ����Դ��
�����Ѷȣ�һ��
3���ƶ��� A��B��C��D����Ԫ��ԭ�ӵĺ˵������������С��20�����䵥�ʼ���Ӧ�Ļ������ܷ������·�Ӧ��ϵ��
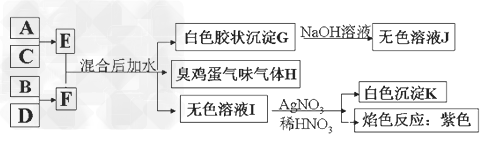
��1��д��F�ĵ���ʽ____________��
��2������H�ж�������Na2CO3��Һ���գ�����������ʽ�Σ��÷�Ӧ�Ļ�ѧ����ʽΪ��________________��
��3������E��ˮ��Һ�����գ����յõ��Ĺ���Ϊ____________,?ԭ��Ϊ_______________,??____________��(�û�ѧ��Ӧ����ʽ����ʾ)?
��4�������£���F��ˮ��Һ�м���������Ũ�ȵ����ᷴӦ��������Һ��PH��7�������Һ������Ũ����С�����˳��Ϊ��_______________��
��5��������H���ڿ����г��ȼ�տɵõ�����������BO2��BO2��������������Ӧ��2BO2+O2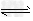 2BO3����һ���̶��ݻ�Ϊ2L���ܱ������г���0.20?mol��BO2��0.10mol��O2������Ӻ�ﵽƽ�⣬��������к�BO3Ϊ0.18mol����
2BO3����һ���̶��ݻ�Ϊ2L���ܱ������г���0.20?mol��BO2��0.10mol��O2������Ӻ�ﵽƽ�⣬��������к�BO3Ϊ0.18mol����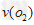 ?=?________?mol��L-1��min-1��������ͨ��0.20mol?BO2��0.10mol?O2���ٴδﵽ��ƽ���BO3�����ʵ�������__________֮�䡣
?=?________?mol��L-1��min-1��������ͨ��0.20mol?BO2��0.10mol?O2���ٴδﵽ��ƽ���BO3�����ʵ�������__________֮�䡣
�ο��𰸣���1��![]() ���������
���������
�����Ѷȣ�һ��
4������� ��ͼ��A��J�ֱ�����йط�Ӧ�е�һ�����ʣ����Ǿ�Ϊ��ѧ��ѧ�еij������ʣ���֪A��E��F��J�зֱ���ͬһ��Ԫ�أ�����д���пհף�

��1������A��ԭ�ӽṹʾ��ͼ______��
��2��ָ��G��Ԫ�����ڱ��е�λ�ù�ϵ______
��3��д��B��C��Ӧ�����ӷ���ʽ��______
��4��д��A?��F������Ӧ�Ļ�ѧ����ʽ______��
�ο��𰸣���A�������ᷴӦ������Ӧ����E�������A����������AΪA
���������
�����Ѷȣ�һ��
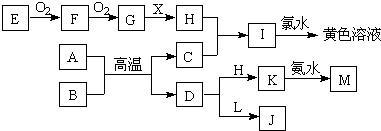
5������� ���п�ͼ��ʾ��ת����ϵ�У�A��C��Ϊ�����Ľ������ʣ�A��C�����H��Ũ��Һ�о��ᷢ���ۻ���EΪ����ǽ������ʣ�BΪ��ɫ���������XΪ������ɫҺ�壮L��ɫΪ��ɫ������ʹ��̪��죨��Ӧ���������ɵ�ˮ��������������ȥ����
��ش��������⣺
��1����̼����0.04%��2.3%֮���C�ĺϽ���Ŀǰ������ʹ�������ĺϽ����ֺϽ���______��
A�����Ͻ�???????????B����ͭ????????????C������?????????D����
��2������������ɫ��Һ�������ӵķ�����______��
��3��I��������Ӧ�����ӷ���ʽΪ______��
��4��A��BӦ����C��D�Ļ�ѧ����ʽΪ______��
��5��D��L��Ӧ�Ļ�ѧ����ʽΪ______��
�ο��𰸣���1����̼����0.04%��2.3%֮�����Ͻ�Ϊ�֣��ʴ�Ϊ��
���������
�����Ѷȣ�һ��