��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���и��������У�����Һ�в��ܴ����������
A.H+��Cl-��Na+��NO3-
B.Ag+��NO3-��Cl-��Na+
C.Ca2+��Na+��Cl-��K+
D.Na+��H+��Cl-��SO42-
�ο��𰸣�B
�����������������������֮���ܽ������ˮ�����塢�����ȣ�������֮�䲻������Ӧ���������ܴ������棬�Դ������
���A����������֮�䲻��Ӧ���ܹ��棬��A��ѡ��
B����Ag+��Cl-�ܽ�����ɳ��������ܹ��棬��Bѡ��
C����������֮�䲻��Ӧ���ܹ��棬��C��ѡ��
D����������֮�䲻��Ӧ���ܹ��棬��D��ѡ��
��ѡB��
���������⿼�����ӵĹ��棬��Ϥ���ֽⷴӦ�����������ǽ����Ĺؼ�����Ŀ�ϼ�
�����Ѷȣ�һ��
2��ѡ���� �����������ʵ����ͬһԭ�����͵���
A.���������͵���������ʹʪ��ĵ��۵⻯����ֽ����
B.����������������ʹƷ����Һ��ɫ
C.���ͣ�NH4��2SO4��Һ�ͱ���CuSO4��Һ����ʹ��������Һ��������
D.�����£���Ƭ����Ƭ����Ũ�����ж��ܳ��ֶۻ�����
�ο��𰸣�D
���������������A������������ʪ��ĵ��۵⻯����ֽ����������ԭ��Ӧ���ɵⵥ�ʣ��ⵥ�������۱�����
B�����������ǿ�����ԣ����������ܺ���ɫ���ʷ�Ӧ������ɫ���ʣ�
C�����ݵ����ʵ������ͱ��Է�����
D�����ݽ����Ķۻ�������
���A������������ʪ��ĵ��۵⻯����ֽ����������ԭ��Ӧ���ɵⵥ�ʣ��ⵥ�������۱���������������͵���������ʹʪ��ĵ��۵⻯����ֽ������ԭ����ͬ����A����
B��������ˮ��Ӧ���ɵĴ��������ǿ�����ԣ���ʹƷ����Һ��ɫ�����������ܺ���ɫ���ʷ������Ϸ�Ӧ������ɫ���ʶ�ʹƷ����Һ��ɫ�����ڷ�������ԭ��Ӧ������Ư��ԭ����ͬ����B����
C�����ͣ�NH4��2SO4��Һ�ͱ���CuSO4��Һ����ʹ��������Һ����������ǰ���Ƿ��������������Ƿ������ԣ���C����Ӧԭ����ͬ����C����
D�������£���������Ũ���ᡢŨ���ᷢ���ۻ���Ӧ�����Գ����£���Ƭ����Ƭ����Ũ�����ж�����������Ӧԭ����ͬ����D��ȷ��
��ѡD��
���������⿼����Ԫ�ػ���������ʣ���Ŀ�ѶȲ������������ʵĿ��飬ע���������ʹ������Ư��ԭ����ͬ������������ʹ���ָʾ����ɫ��
�����Ѷȣ�һ��
3��ѡ���� ���б仯��������������Ӧ����
A.HCl��H2
B.Mg��Mg2+
C.Cl-��AgCl
D.CuO��Cu
�ο��𰸣�B
�������������������������Ӧʱ����������Ԫ�صĻ��ϼ�Ӧ���ߣ��ڷ�Ӧ��ʧȥ���ӱ�������
���A��HԪ�ػ��ϼ۽��ͣ�����ԭ�����ڻ�ԭ��Ӧ����A����
B��MgԪ�ػ��ϼ����ߣ�������������������Ӧ����B��ȷ��
C��ClԪ�ػ��ϼ�û�з����仯������������ԭ��Ӧ����C����
D��CuԪ�ػ��ϼ�û�з����仯������������ԭ��Ӧ����D����
��ѡB��
���������⿼��������ԭ��Ӧ����Ŀ�ѶȲ���ע���ж�������Ӧ����ԭ��Ӧ��Ԫ�ػ��ϼ۱仯�Ĺ�ϵ���ι̰�����ظ��
�����Ѷȣ�һ��
4��ѡ���� ���б�ʾ��Ӧ��ѧ��Ӧ�����ӷ���ʽ��ȷ����
A.����NH3ͨ��1.2mol/L FeCl3��Һ��Fe3++3NH3?H2O=Fe��OH��3�����壩+3NH4+
B.Ư����Һ��ͨ�����CO2���壺Ca2++2ClO-+CO2+H2O=CaCO3��+2HClO
C.����Cl2ͨ��1.0mol/L Na2SO3��Һ�У�2SO32-+Cl2=2S��+2ClO3-
D.��ȩ�м���������Һ��ˮԡ���ȣ�CH3CHO+2Ag��NH3��2++2OH-2Ag��+CH3COO-+NH4++3NH3+H2O
�ο��𰸣�D
���������������A����Ӧ���ɳ�����
B����Ӧ����̼����ƺ�HClO��
C������������ԭ��Ӧ��������������Ӻ������ӣ�
D������������Ӧ������Ag������李�������ˮ��
���A������NH3ͨ��1.2mol/L FeCl3��Һ�����ӷ�ӦΪFe3++3NH3?H2O=Fe��OH��3��+3NH4+����A����
B��Ư����Һ��ͨ�����CO2��������ӷ�ӦΪClO-+CO2+H2O=HCO3-+HClO����B����
C������Cl2ͨ��1.0mol/L Na2SO3��Һ�е����ӷ�ӦΪH2O+SO32-+Cl2=SO42-+2Cl-+2H+����C����
D����ȩ�м���������Һ��ˮԡ���ȵ����ӷ�ӦΪCH3CHO+2Ag��NH3��2++2OH-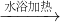 2Ag��+CH3COO-+NH4++3NH3+H2O����D��ȷ��
2Ag��+CH3COO-+NH4++3NH3+H2O����D��ȷ��
��ѡD��
���������⿼�����ӷ�Ӧ����ʽ��д�������жϣ���ȷ�����Ļ�ѧ��Ӧ�ǽ��Ĺؼ���ע�⽺����Ʊ���ѡ���е�������ԭ��Ӧ��ѡ��CΪ�����״��㣬��Ŀ�Ѷ��еȣ�
�����Ѷȣ�����
5��ѡ���� ��2mol?NaHCO3��һ������Na2O2�����ϣ��ڼ��������������ַ�Ӧ��õ��Ĺ��壬���ⶨNa2O2��ʣ�࣬������������ʵ���Ϊ
A.1��2mol֮��
B.1��4mol֮��
C.2��4mol֮��
D.����4mol
�ο��𰸣�B
���������������2molNaHCO3�ֽ�����1molNa2CO3��1molH2O��1molCO2�����ɵ�1molH2O��1molCO2���Na2O2���巴Ӧ���ɲ��ü�ֵ�������㣮
��𣺼��Ⱥ�����Ӧ���£�
2NaHCO3 Na2CO3 +H2O+CO2����
Na2CO3 +H2O+CO2����
2mol????? ?1mol 1mol 1mol
2Na2Oz+2CO2�T2Na2CO3+O2
1mol 1mol
2Na2Oz+2H2O�T4NaOH+O2��
1mol 2mol
�ɷ�Ӧ����ʽ��֪������Na2O2�������ʱ��2mol NaHCO3�ֽ�����1molNa2CO3��
��2mol NaHCO3�ֽ����ɵ�H2O��CO2��������Na2O2����ʱ����������1mol Na2CO3��2molNaOH�����Թ���������4mol��
��ѡ��B��
���������⿼����̼�����Ƶ����ʼ��������Ƶ����ʼ��йؼ��㣮���巴Ӧԭ�����ҳ�����֮��Ĺ�ϵ�ǽ���Ļ��������ڷ�Χ�����Ŀ�������ü�ֵ�����м��㣮
�����Ѷȣ�����