微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (1)炒过菜的铁锅未及时洗净,不久便会因腐蚀而出现红褐色锈斑。请回答:
①铁锅的锈蚀是____腐蚀(填“析氢”或“吸氧”)。
②写出铁锅腐蚀正极的电极反应式:____。
(2)①某同学用碳棒、铜棒和稀硫酸为原材料,实现了在通常条件下不能发生的反应:
Cu+H2SO4(稀)==CuSO4+H2↑。请画出能够实现这一反应的装置示意图。
②某同学在做一定条件下铜与稀硫酸的反应实验时,看到碳棒上有气泡产生,但铜棒却没有被腐蚀。请你分析其原因:____。
参考答案:(1)①吸氧;②2H2O+O2+4e-==4OH-
本题解析:
本题难度:一般
2、选择题 下列关于铜电极的叙述,不正确的是 ( )
A.电池反应为2Ag++Cu===2Ag+Cu2+的原电池中,铜作负极
B.电解法精炼粗铜时,精铜作阴极
C.电解饱和食盐水制H2、Cl2、NaOH时,铜作阳极
D.在镀件上镀铜时,铜作阳极
参考答案:C
本题解析:
试题分析:铜是活性电极,电解饱和食盐水时,铜不能作为阳极,只能作为阴极。否则溶液中的氯离子就不能再放电,即选项C不正确,其余选项都是正确的,答案选C。
点评:在判断电解产物时,首先判断阳极电极材料。如果是活性电极,则电极本身失去电子。如果是惰性电极,则溶液中的阴离子失去电子。而阴极是溶液中的阳离子得到电子,据此可以进行有关判断。
本题难度:一般
3、填空题 (8分)I.炒过菜的铁锅未及时洗净,不久便会因腐蚀而出现红褐色锈斑。请回答:
(1)铁锅的锈蚀是???????腐蚀(填“析氢”或“吸氧”)。
(2)写出铁锅腐蚀正极的电极反应式:??????????????????????????????????。
II.(1)某同学运用所学知识,自选材料设计实验,实现了在通常条件下不能发生的反应:Cu+H2SO4(稀)=CuSO4+H2↑。
请你在方框内画出能够实现这一反应的装置图。

(2)某同学在做一定条件下铜与稀硫酸的反应实验时,看到碳棒上有气泡产生,但铜棒却没有被腐蚀。请你分析其原因:???????????????????????????????????????????????????????????????????????????。
参考答案:I.(1)吸氧(1分)???
(2)2H2O+O2+4
本题解析:
试题分析:I.(1)铁锅表面溶液为中性,发生吸氧腐蚀。
(2)正极上O2得电子:2H2O+O2+4e-= 4OH-。
II.(1)根据化学方程式:Cu+H2SO4(稀)=CuSO4+H2↑,Cu失电子应为阳极,所以Cu与外加电源的正极相连,电解质为H2SO4溶液,进而可画出装置图,
(2)铜棒却没有被腐蚀,说明铜棒没有作阳极,可能为:两极与电源的正负极接反了,或铜棒接电源的负极了等。
本题难度:一般
4、填空题 下图中a为生铁,A烧杯中放入苯,B烧杯中为1 mol・L-1的稀硫酸,C烧杯中为海水。
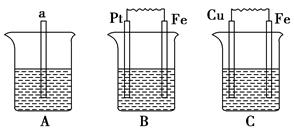
(1)B中Pt极的电极反应式为________。
(2)C中Cu极的电极反应式为________,Cu极附近溶液的pH________(填“增大”、“减小”或“不变”)。
(3)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是________。
(4)要使B中的铁难被腐蚀,可将B中的稀硫酸改为________。
参考答案:(1)2H++2e-=H2↑
(2)2H2O+O2+4
本题解析:(1)B中Pt极的电极反应式为2H++2e-=H2↑。(2)C中Cu极是正极,发生还原反应,电极反应式为2H2O+O2+4e-=4OH-,Cu极附近溶液的pH增大。(3)由于Fe与Pt的活动性差距比Fe与Cu大,故B中反应速率快,而A中物质是苯,铁不易被腐蚀,故腐蚀速率由快到慢的顺序是B>C>A。(4)要使B中的铁难被腐蚀,可将B中的稀硫酸改为非电解质溶液,如酒精、苯、四氯化碳等。
本题难度:一般
5、选择题 如下图所示,下列叙述正确的是 (???)??
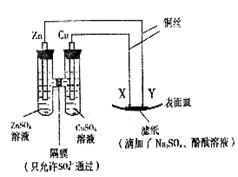
A.Y为阴极,发生还原反应
B.X为正极,发生氧化反应
C.Y与滤纸接触处有氧气生成
D.X为滤纸接触处变红
参考答案:A
本题解析:
试题分析:B、Cu为正极,X为阳极,故错;C、Y是阴极,发生还原反应,生成氢气;D、X为阳极,发生氧化反应,OH-反应生成氧气,X为滤纸接触处不变红,故错。故选A。
点评:本题考查的是电解池的工作原理的知识,题目难度不大,注意原电池和电解池的区别,熟悉原电池和电解池的工作原理是解题的关键。
本题难度:一般